 Synthèse du paracétamol ou de lacétanilide CORRECTION
Synthèse du paracétamol ou de lacétanilide CORRECTION
Synthèse de l'acétanilide : (Groupes impairs). 1)&2) Voir I. 3) Rendement : • On détermine la masse d'acétanilide attendu. Pour cela il faut savoir quel est
 Synthèse du paracétamol ou de lacétanilide
Synthèse du paracétamol ou de lacétanilide
Extraire et exploiter des informations : - sur l'utilisation de réactifs chimiosélectifs. - sur la protection d'une fonction dans le cas de la synthèse
 D.S. n° 1
D.S. n° 1
Dans la synthèse décrite dans la suite on remplacera l'acide éthanoïque par un dérivé de cet acide : l'anhydride éthanoïque. Au lycée
 CORRECTİON DES EXERCİCES – C13
CORRECTİON DES EXERCİCES – C13
Synthèse de l'acétanilide. 1. L'anhydride éthanoïque est corrosif : manipulation avec blouse gants et lunettes de protection. L'aniline est toxique et
 EXERCICE I : SYNTHÈSE DUN FÉBRIFUGE : LACÉTANILIDE ( 4
EXERCICE I : SYNTHÈSE DUN FÉBRIFUGE : LACÉTANILIDE ( 4
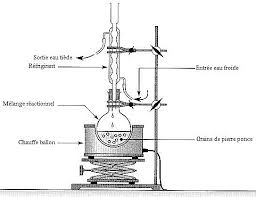
SYNTHESE D'UN FÉBRIFUGE … correction. 1.1.a. Montage à reflux : 1.1.b. Le L'acétanilide étant très peu soluble dans l'eau froide il cristallise. 1.1 ...
 TRAVAUX PRATIQUES DE CHIMIE ORGANIQUE FILIERE SMC S5
TRAVAUX PRATIQUES DE CHIMIE ORGANIQUE FILIERE SMC S5
SYNTHESE DE L'ACIDE BENZOIQUE. I-. Principe. La réaction haloforme est une réaction caractéristique des cétones α-méthylées. (R-CO-CH3).Plutôt que d'utiliser la
 QUATRE SATELLITES TERRESTRES ARTIFICIELS PARMI BIEN D
QUATRE SATELLITES TERRESTRES ARTIFICIELS PARMI BIEN D
TS 6 spé. CONTRÔLE DE SCIENCES PHYSIQUES. Durée conseillée : 45 minutes. 12/12/11. Lors de la correction il sera Étape 1 : synthèse de l'acétanilide.
 Corrigé D.S de Spécialité Physique Chimie
Corrigé D.S de Spécialité Physique Chimie
10 déc. 2011 Définir et calculer le rendement de cette synthèse. (3 pts). Le rendement d'une synthèse est le rapport de la masse d'acétanilide obtenue ...
 Thème :
Thème :
Acétanilide. Bilan macroscopique de la synthèse : □ Classe de la réaction (basée sur la comparaison des structures) : Lors de cette transformation chimique le
 Synthèse du paracétamol ou de lacétanilide CORRECTION
Synthèse du paracétamol ou de lacétanilide CORRECTION
TPC15. Chapitre C12 : Sélectivité en chimie organique. Synthèse du paracétamol ou de l'acétanilide. CORRECTION. I. Synthèse du paracétamol : (Groupes pairs).
 Correction dexamen TP Synthèse organique 1.a; Définir les termes
Correction dexamen TP Synthèse organique 1.a; Définir les termes
La réaction de 10 ml l'anhydride éthanoïque avec 5 ml de l'aniline en présence d'acide éthanoïque à 80 Cº conduit à un fébrifuge ( l'acétanilide ). a) C'est
 D.S. n° 1
D.S. n° 1
Étape 1 : synthèse de l'acétanilide. - dans un ballon rodé propre et sec introduire V1 = 15 mL d'acide éthanoïque qui joue ici le rôle de solvant
 A.R.E.
A.R.E.
Deux travaux pratiques sont prévus : la synthèse de chimie organique d'un médicament (3h en salle TP CHIMIE : SYNTHESE D'UN MEDICAMENT - L'ACETANILIDE.
 Thème :
Thème :
Acétanilide ;. • Acide acétylsalicilique ;. • Paracétamol. • CONTEXTUALISATION DES SYNTHESES ORGANIQUES. • PISTES D'EXPLOITATION AVEC LES ELEVES. • COMPETENCES
 Synthèse du paracétamol ou de lacétanilide
Synthèse du paracétamol ou de lacétanilide
Synthèse du paracétamol ou de l'acétanilide. Notions et contenus. Compétences exigibles. Sélectivité en chimie organique. Composé polyfonctionnel : réactif.
 EXERCICE I Synthèse dun fébrifuge: lacétanilide (4 points) spécialité
EXERCICE I Synthèse dun fébrifuge: lacétanilide (4 points) spécialité
L'acétanilide C6H5—NH—CO—CH3 fut l'un des premiers fébrifuges (médicaments combattant la fièvre) synthétisé par l'industrie chimique à partir de l'aniline
 Analyse spectrale Spectres IR
Analyse spectrale Spectres IR
Les corrigés sont rédigés par les professeurs de l'association Labolycée. L'autre produit issu de la synthèse de l'aspirine est l'acide éthanoïque de ...
 Untitled
Untitled
Synthèse de l'acétanilide. 9. Synthèse de la benzocaine. 10. Synthèse du savon. 11. Identification des produits obtenus par des méthodes physicochimiques et
 Correction de Contrôle de TP Synthèse Organique
Correction de Contrôle de TP Synthèse Organique
I. Réaction de synthèse : C'est l'étape ou la réaction étudiée a lieu : Dans un solvant choisi
 SYNTHÈSE D’UN FÉBRIFUGE : L’ACÉTANILIDE
SYNTHÈSE D’UN FÉBRIFUGE : L’ACÉTANILIDE
SYNTHÈSE D’UN FÉBRIFUGE : L’ACÉTANILIDE L’acétanilide C 6 H 5 — NH — CO — CH 3 fut l’un des premiers fébrifuges (médicaments combattant la fièvre) synthétisé par l’industrie chimique à partir de l’aniline et du vinaigre (solution aqueuse d’acide éthanoïque) C’est un solide blanc
 TPC1 4 Synthèse du paracétamol ou de l’acétanilide - Labo TP
TPC1 4 Synthèse du paracétamol ou de l’acétanilide - Labo TP
2) Réaliser la synthèse du paracétamol ; une synthèse s’effectue en plusieurs étapes : - Synthèse du produit brut - Séparation du produit d’intérêt des autres espèces - Purification par recristallisation - Identification du produit obtenu 3) Calculer le rendement de la réaction ? = masse de produit obtenu
 Synthèse du paracétamol ou de l’acétanilide CORRECTION
Synthèse du paracétamol ou de l’acétanilide CORRECTION
Synthèse du paracétamol ou de l’acétanilide CORRECTION I Synthèse du paracétamol : (Groupes pairs) 1) Il est nécessaire de porter une blouse des lunettes de protection et d’utiliser au maximum la hotte aspirante 2) Pour la purification par recristallisation on dissout le produit brut dans de l’eau chaude Les
 Searches related to synthèse de l acétanilide corrigé PDF
Searches related to synthèse de l acétanilide corrigé PDF
Acétanilide Bilan macroscopique de la synthèse : O O Classe de la réaction (basée sur la comparaison des structures) : Lors de cette transformation chimique le groupe caractéristique amino du réactif principal (aniline) est modifié : il est remplacé par un groupe amide : il s’agit d’une éat ion de substitution
Comment faire la synthèse de l’acétanilide ?
Étape 1 : synthèse de l’acétanilide. dans un ballon rodé propre et sec, introduire V1 = 15 mL d’acide éthanoïque qui joue ici le rôle de solvant, V2 = 15,0 mL d’anhydride éthanoïque, V3 = 10,0 mL d’aniline et quelques grains de pierre ponce ;
Quels sont les bienfaits de l’acétanilide ?
développement photographique (au XIXe siècle). En outre, l’acétanilide a des propriétés analgésiques et réduit la fièvre. Elle se classe dans la même catégorie de médicaments que le paracétamol. Elle est souvent prescrite à de nombreux patients et on la trouve dans la plupart des pharmacies.
Comment fonctionne l'acétanilide ?
Ainsi, il existe des structures de résonance où une charge négative se déplace dans l'anneau, et une autre où elle réside dans l'atome O. En conséquence de cette «asymétrie électronique» -qui vient de la main de l'asymétrie moléculaire-, l'acétanilide il interagit de manière intermoléculaire par des forces dipôle-dipôle.
Qu'est-ce que le Acétanilide ?
Le acétanilide (C8H9NO) est un amide aromatique qui reçoit plusieurs noms supplémentaires: N-acétylarylamine, N-phénylacétamide et acétanil. Il se présente comme un solide inodore sous forme de paillettes, sa nature chimique est l'amide, et en tant que tel peut former des gaz inflammables en réagissant avec des agents réducteurs puissants.

Analyse spectrale
Spectres IR
5 Extraits de sujets corrigés du bac S
© http://labolycee.org
La spectroscopie infrarouge : un moyen de déterminer les groupes https://youtu.be/U0Hu3-J0igE Animation par Ostralo.net http://chimie.ostralo.net/spectreIR/ Les corrigés sont rédigés par les professe Ces corrigés sont accessibles gratuitement et sans inscription sur http://labolycee.org Contacts : https://twitter.com/Labolycee ; https://www.facebook.com/labolycee/ ; labolycee@labolycee.org Les exercices de bac sont conçus à partir de la colonne Compétences exigibles.Notions et contenus Compétences exigibles
Spectres IR
https://youtu.be/1ZQXEZKBKTYIdentification de liaisons à l'aide du
nombre d'onde correspondant ; détermination de groupes caractéristiques.Mise en évidence de la liaison
hydrogène. Exploiter un spectre IR pour déterminer des groupes caractéristiques à l'aide de tables de données ou de logiciels. Associer un groupe caractéristique à une fonction dans le cas des alcool, aldéhyde, cétone, acide carboxylique, ester, amine, amide. Connaître les règles de nomenclature de ces composés ainsi que celles des alcanes et des alcènes. https://youtu.be/icmXwHywn9g Identification d'une molécule organique par IR et RMNde 10 min, réalisé par la fondation Maison de la Chimie et le CNDP : https://youtu.be/swvc0fQL5RQ Extrait 1 Bac S 2013 Amérique du nord http://labolycee.org EXERCICE I : ASPIRINE ET PRÉVENTION CARDIOVASCULAIRE (8,5 points)Accès à la correction
2H4O2.
2.2.1. Donner la formule semi-
e éthanoïque.2.2.2. Les spectres infrarouges de ces deux espèces chimiques sont regroupés dans le
document 3 ci-dessous. Une table de données de spectroscopie infrarouge est également fournie (document 4). que en justifiant.Document 3 :
Document 4 : table de données pour la spectroscopie IR. famille liaison -1) cétone C = O 1705 - 1725 aldéhyde Ctri H C = O2700 -2900
1720 - 1740
acide carboxylique O H C = O2500 - 3200
1740 - 1800
ester C = O 1730 - 1750 alcool O HliéO Hlibre
3200 3450
3600 - 3700
Extrait 2 Bac S 2013 Amérique du sud http://labolycee.orgEXERCICE II. LES DANGERS DE L'ALCOOL (7,5 points)
Document 1
1. Spectroscopie
On se propose d'étudier la structure et les fonctions organiques de ces molécules par spectroscopie.
http://www.sciences-edu.net Document 2a : Spectroscopie Infrarouge en phase liquide. Spectre IR1On trouve dans un document publié par l'Institut suisse de prévention de l'alcoolisme (ISPA) les
informations suivantes : Quand une personne consomme de l'alcool, celui-ci commence immédiatement à passer dans le sang. Plus le passage de l'alcool dans le sang est rapide, plus le taux d'alcool dans le sangaugmentera rapidement, et plus vite on sera ivre. L'alcool est éliminé en majeure partie par le foie.
Dans le foie, l'alcool est éliminé en deux étapes grâce à des enzymes. Dans un premier temps,
l'alcool est transformé en éthanal par l'enzyme alcool déshydrogénase (ADH). L'éthanal est une
substance très toxique, qui provoque des dégâts dans l'ensemble de l'organisme. Il attaque les
membranes cellulaires et cause des dommages indirects en inhibant le système des enzymes.Dans un deuxième temps, l'éthanal est métabolisé par l'enzyme acétaldéhyde déshydrogénase
(ALDH). www.sfa-ispa.chAlcool pur : Ethanol : C2H6O
Enzyme ADH
Ethanal C2H4O
Dégradation ultérieure...
Synthèse du cholestérol
http://www.sciences-edu.net Document 2b : Spectroscopie Infrarouge en phase liquide. Spectre IR2Liaison C - C C - O C = O (carbonyle) C - H O - H
Nombre d'onde
(cm-1) 1000-1250 1050-1450 1650-1740 2800-3000 3200-3700 Document 2c : Table de données pour la spectroscopie IR1.1. Le document 1 évoque les molécules d'éthanol et d'éthanal : représenter en formule semi-développée
ces deux molécules et encadrer leurs fonctions caractéristiques.1.2. Quel est le nom du groupe fonctionnel porté par l'éthanol ? À quelle famille appartient cette molécule ?
1.3. Quel est le nom du groupe fonctionnel porté par l'éthanal ? À quelle famille appartient cette molécule ?
1.4. En utilisant les données spectroscopiques du document 2, associer chaque spectre infrarouge (IR) à la
molécule correspondante en justifiant.Accès à la correction
Extrait 3 Bac S 2015 Antilles Guyane http://labolycee.orgLa benzocaïne (4- ique local
leil, mais onla trouve aussi dans de nombreuses autres préparations : pastilles contre les maux de gorge,
produits gingivaux contre les douleurs dentaires. Dasynthétiser de la benzocaïne. Pour cela quatre grandes tâches devront être réalisées :
la vérification de la pureté du réactif ; ntification du produit obtenu.4. Identification du produit formé
-aminobenzoïque et du produit obtenu. Associer à chaque molécule son spectre IR en justifiant. Accès à la correctionDocument 1 : La synthèse de la benzocaïne
La benzocaïne est préparée à partir du toluène en plusieurs étapes.La première étape débute par une nitration du toluène, suivie par une hydrogénation catalytique
en présence de palladium afin de réduire le groupe nitro NO2 en groupe NH2.On procède ensuite à une oxydation sélective, par du permanganate de potassium, pour obtenir
un ouvrage universitaire de chimie organique (J. Clayden & al. Chimie organique)Accès à la correction
Document 3 : Analyse du produit obtenu
Spectres infraroug-aminobenzoïque et du produit obtenuTable spectroscopique IR simplifiée :
Liaison m-1) Intensité
O-H alcool libre 3500 - 3700 forte, fine
O-H alcool lié 3200 - 3400 forte, large
O-H acide carboxylique 2500 - 3200 forte à moyenne, largeN-H amine 3100 - 3500 moyenne
N-H amide 3100 - 3500 forte
N-H amine ou amide 1560 - 1640 forte ou moyenne
Ctri - H 3000 - 3100 moyenne
Ctét - H 2800 - 3000 forte
C = O ester 1700 -1740 forte
C = O amide 1650 - 1740 forte
C = O aldéhyde et cétone 1650 - 1730 forte
C = O acide 1680 - 1710 forte
Remarque :
Ctri -à-dire relié à trois voisins.
Ctét -à-dire relié à quatre voisins.
Extrait 4 Bac S 2013 Pondichéry http://labolycee.orgExercice II Molécul
est une molécule de formule brute C13H18O2. Son nom en nomenclature officielle est acide2-(4-isobutylphényl)propanoïque.
De par ses propriétés anti-inflammatoire, antalgique et antipyrétique, elle constitue le principe actif de divers médicaments. Cet exercice comporte trois parties indépendantes conduisant à étudier la structure de la moléculeèse dans le cadre de la chimie
Partie 1 : La molécul
Les spectroscopies IR (infrarouge) et de RMN (résonance magnétique nucléaire) en sont deux
exemples.1.3.1. IR (document 1) en
exploitant les données du document 2.Accès à la correction
CH H3C C O OH CH3 CHCH3 CH2
C CH CH C HC HCFormule semi-développée
Document 2
iquesDocument 1
Extrait 5 Bac S 2013 Liban Exercice I. ACIDE LACTIQUE ET MÉDECINE ANIMALE (7 points) http://labolycee.org1. Lacide lactique
La formule semi-développée de lacide lactique est la suivante : H3C CH C1.2. Analyse spectroscopique
Accès à la correction
1.2.1. Parmi les spectres IR proposés dans le document 1 ci-après, choisir en justifiant celui
correspondant à lacide lactique. Accès à la correctionDocument 1 : Spectres IR
Spectre IR n°1
Spectre IR n°2
Donnée : bandes dabsorption en spectroscopie IRLiaison CC C=O OH (acide
carboxylique) CH OH (alcool)Nombre
1) 1000 - 1250 1700 - 1800 2500 - 3200 2800 - 3000 3200 - 3700
O OH OH Extrait 1 Bac S 2013 Amérique du nord Correction © http://labolycee.org EXERCICE I : ASPIRINE ET PRÉVENTION CARDIOVASCULAIRE (8,5 points)2.2.1. (0,5 pt)
Retour vers le sujet
Acide éthanoïque méthanoate de méthyle2.2.2. (0,5 pt)
thanoate de méthyle. Extrait 2 Bac S 2013 Amérique du sud CORRECTION © http://labolycee.orgEXERCICE II. LES DANGERS DE L'ALCOOL (7,5 points)
1. Spectroscopie
1.1. Formules semi-développées Retour vers le sujet
Éthanol Éthanal
CH3CH2OH
1.2. Groupe fonctionnel hydroxyle 1.3. Groupe fonctionnel carbonyle
Famille : alcool Famille : aldéhyde
1.4. Le spectre IR2 montre une bande large et intense autour de 3300 cm1 qui caractérise le groupe
anol.Le spectre IR1 montre une bande fine et intense autour de 1700 cm1 qui caractérise le groupe carbonyle de
thanal. CH3 C O OH CH O O CH3Bande à 2500 3200 cm-1
Caractéristique de la liaison OH
Bande à 1740 1800 cm-1
Caractéristique de la liaison C = O
Bande à 1730 1750 cm-1
Caractéristique de la liaison
C =0 de
CH3 CH
O Extrait 3 Bac S 2015 Antilles Guyane http://labolycee.org4. Identification du produit formé
4.1. acide 4-aminobenzoïque :
(0,5 + 0,5) de la benzocaïne :Retour vers le sujet
Pour pouvoir attribuer ces 2 spectres, il faut chercher les différences entres ces 2 molécules : une
fonction acide carboxylique pour la 1ère, une fonction ester pour la 2nde. La d importante pour attribuer les spectres. On retrouve dans le spectre 1, une bande large pour la liaison O-- aminobenzoïque entre 2500 et 3200 cm-1 dans le spectre 2. -aminobenzoïque est le spectre 1. Extrait 4 Bac S 2013 Physique Chimie Pondichéry CORRECTION © http://labolycee.orgExercice
1.3.1. (0,5 pt) La bande n°1 est fine, de forte intensité et correspond à u
1700 cm-1 e.
(0,5 pt) La bande n°2 est large et centrée autour de = 3000 cm-1, elle peut caractériser les liaisons
C H ou/et la liaison O-
Retour vers le sujet
Extrait 5 EXERCICE I : ACIDE LACTIQUE ET MÉDECINE ANIMALE (7 points)CORRECTION © http://labolycee.org
1.2.1. (0,5 pt) Analyse spectroscopique Retour vers le sujet
Le spectre n°1 correspond à l sente que dans le spectre n°1.Bande fine vers 1750 cm-1
caractéristique de la liaison C = OBande large qui peut englober la
liaison O H (alcool) entre 3200 et3700 cm-1 et la liaison O H de
lique (2500 3200 cm-1), non présente dans le deuxième spectrequotesdbs_dbs31.pdfusesText_37[PDF] fables de la fontaine théâtre
[PDF] synthèse de laspirine ? partir de lacide salicylique
[PDF] la cigale et la fourmi version theatre
[PDF] synthèse de lacétanilide tp
[PDF] mettre en scène un conte ? lécole
[PDF] synthèse aspirine tp
[PDF] les fables de la fontaine mise en scene par robert wilson
[PDF] schéma narratif le renard et la cigogne
[PDF] le renard et la cigogne analyse des personnages
[PDF] comment les plantes se défendent elles
[PDF] le torrent et la rivière date
[PDF] telecharger e.t l'extra terrestre dvdrip
[PDF] les structures et mécanismes de défense de l'acacia caffra
[PDF] morale du torrent et la rivière
