 4. CHROMATOGRAPHIE LIQUIDE
4. CHROMATOGRAPHIE LIQUIDE
• la chromatographie de partage est la technique de chromatographie liquide la plus chromatographie en phase inverse. • 4 solvants sont utilisés pour ...
 LES CHROMATOGRAPHIES
LES CHROMATOGRAPHIES
La chromatographie de partage fonctionne par partage de solutés entre deux phases non La chromatographie sur colonne présente plusieurs inconvénients :.
 TECHNIQUES: Principes de la chromatographie
TECHNIQUES: Principes de la chromatographie
La chromatographie d'adsorption est basée sur le partage des solutés entre l'adsorbant solide fixe et la phase mobile. Chacun des solutés est soumis à une force
 Extraction et séparation de la chlorophylle
Extraction et séparation de la chlorophylle
Il servira à la chromatographie de partage sur colonne. On obtient de la chlorophylle pure collée au fond de l'Erlenmeyer. • Resolubiliser la chlorophylle
 Amélioration instrumentale de la chromatographie de partage
Amélioration instrumentale de la chromatographie de partage
3 mai 2018 Pour cela nous proposons d'introduire la chromatographie liquide-liquide ou chromatographie de partage centrifuge dont le principe sera décrit ...
 Les techniques Chromatographiques 1.1. Introduction 1.3. Historique
Les techniques Chromatographiques 1.1. Introduction 1.3. Historique
La chromatographie de partage : C'est une chromatographie liquide-liquide. D. 2. Le Principe de la chromatographie d'exclusion. Cette technique permet la ...
 APPLICATIONS DE LA CHROMATOGRAPHIE DE PARTAGE SUR
APPLICATIONS DE LA CHROMATOGRAPHIE DE PARTAGE SUR
guide dans son isolement par Chromatographie de partage sur colonne d'ami- don. La figure 6 reproduit le chromatogramme en deux dimensions (réalisé. Page 17
 Master de lInstitut Supérieur des Sciences Agronomiques
Master de lInstitut Supérieur des Sciences Agronomiques
Chromatographie de partage centrifuge (CPC). 2.1. Principe. La Chromatographie de partage centrifuge est une technique de chromatographie liquide-liquide sans
 CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
CHROMATOGRAPHIE LIQUIDE - Académie des Sciences et Lettres
Représentation schématique des interactions mises en jeu dans la chromatographie en phase inverse. Le coefficient de distribution (ou coefficient de partage)
 GRADIENT DE POLARITE EN CHROMATOGRAPHIE DE
GRADIENT DE POLARITE EN CHROMATOGRAPHIE DE
de partage de BERGSTR~I
 [PDF] TECHNIQUES: Principes de la chromatographie - Eli Zysman-Colman
[PDF] TECHNIQUES: Principes de la chromatographie - Eli Zysman-Colman
La chromatographie d'adsorption est basée sur le partage des solutés entre l'adsorbant solide fixe et la phase mobile Chacun des solutés est soumis à une force
 [PDF] La chromatographiepdf
[PDF] La chromatographiepdf
Principe La chromatographie repose sur l'entraînement d'un échantillon dissous par une La phase stationnaire en chromatographie de partage doit être
 [PDF] NOTIONS FONDAMENTALES DE CHROMATOGRAPHIE
[PDF] NOTIONS FONDAMENTALES DE CHROMATOGRAPHIE
On distingue deux types de chromatographie: sur colonne et planaire CLPgreffée Groupemt lié chimiquement à un gel Partage entre liq et surface
 [PDF] 1 Définition 2 Buts de la chromatographie 21 Objectif analytique
[PDF] 1 Définition 2 Buts de la chromatographie 21 Objectif analytique
C'est une méthode de séparation non destructrice en son principe substrat agissant par partage (chromatographie liquide - liquide : CLL)
 [PDF] CHROMATOGRAPHIE - AC Nancy Metz
[PDF] CHROMATOGRAPHIE - AC Nancy Metz
Chromatographie en phase gazeuse (CPG): Le principe de la séparation par C P G consiste à partager l'échantillon à analyser entre deux phases L'une de ces
 [PDF] Chromatographie - L3 Chimie Dijon
[PDF] Chromatographie - L3 Chimie Dijon
Le principe repose sur l'équilibre de concentrations des composés présents La chromatographie liquide-liquide (CLL) ou chromatographie de partage :
 [PDF] LES CHROMATOGRAPHIES
[PDF] LES CHROMATOGRAPHIES
la chromatographie de partage (LLC GLC) lorsque la phase stationnaire est un imprègne un support en principe inerte ou est greffée par liaison
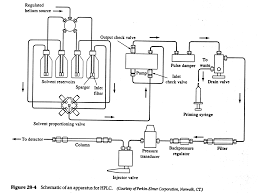
 [PDF] HPLC Principe et appareillage
[PDF] HPLC Principe et appareillage
20 jan 2010 · La chromatographie permet la séparation ou la purification d'un ou de rapport à l'équilibre est appelé coefficient de partage K
 [PDF] LES CHROMATOGRAPHIES
[PDF] LES CHROMATOGRAPHIES
La chromatographie de partage fonctionne par partage de solutés entre deux phases non miscibles ; l'une mobile et l'autre stationnaire La phase stationnaire
 [PDF] 4 CHROMATOGRAPHIE LIQUIDE
[PDF] 4 CHROMATOGRAPHIE LIQUIDE
La chromatographie de partage convient très bien à la séparation de molécules très polaires de masses moléculaires inférieures à 3000 et aux homologues d'une
 cours sur le chapitre 3: Chromatographie de partage
cours sur le chapitre 3: Chromatographie de partage
Principe de la chromatographie de partage La phase stationnaire et la phase mobile sont liquides Elle est basée sur la différence de solubilité du soluté
 [PDF] La chromatographiepdf
[PDF] La chromatographiepdf
Principe La chromatographie repose sur l'entraînement d'un échantillon dissous par une La phase stationnaire en chromatographie de partage doit être
 [PDF] TECHNIQUES: Principes de la chromatographie
[PDF] TECHNIQUES: Principes de la chromatographie
La chromatographie d'adsorption est basée sur le partage des solutés entre l'adsorbant solide fixe et la phase mobile Chacun des solutés est soumis à une force
 [PDF] [PDF] Cours de Chromatographie
[PDF] [PDF] Cours de Chromatographie
Chromatographie gazeuse : principe et appareillage Adsorption ? Partage ? Paires d'ions ? Échange d'ions ? Exclusion stérique
 Chromatographie de partage - Wikipédia
Chromatographie de partage - Wikipédia
La chromatographie de partage est une méthode de séparation de molécules par chromatographie suivant leur migration/répartition différentielle dans deux
 La chromatographie Planet-Vie
La chromatographie Planet-Vie
15 mai 2012 · La chromatographie de partage en phase gazeuse utilise comme principe de séparation le partage différentiel des molécules à séparer dans les
 [PDF] Chapitre 2 : Chromatographie - opsuniv-batna2dz
[PDF] Chapitre 2 : Chromatographie - opsuniv-batna2dz
? Le principe de la chromatographie consiste à entrainer l'échantillons à l'aide d'un éluant (gazeux ou liquide) appelé phase mobile (PM) qui se déplace au
 [PDF] Chromatographie - L3 Chimie Dijon
[PDF] Chromatographie - L3 Chimie Dijon
Principe : Le principe repose sur l'équilibre de concentrations des composés présents entre deux phases en contact : la phase stationnaire et la phase
Quel est le principe de la chromatographie de partage ?
La chromatographie de partage en phase gazeuse utilise comme principe de séparation le partage différentiel des molécules à séparer dans les deux phases stationnaires et mobiles.15 mai 2012Quel est le principe de la chromatographie ?
La chromatographie est une méthode physico-chimique qui sert à séparer les différentes substances présentes dans un mélange (échantillon en phase homogène liquide ou gazeuse).Quel est le principe CCM ?
Principe. ? Une CCM, c'est quoi ? Il s'agit d'une technique d'analyse qui s'appuie sur les différences d'affinités de substances chimiques entre une phase fixe, la plaque, et une phase mobile, l'éluant. Cette différence va permettre la séparation de ces différentes substances sur la plaque.- La CCM se déroule en trois étapes : préparation de la cuve, préparation de la plaque, et élution. Un cuve de chromatographie se compose de la cuve et d'un couvercle.
TECHNIQUES:
Principes de la
chromatographie 2Définition
La chromatographie est une méthode physique de séparationbasée sur les différentes affinités d'un ou plusieurs composés à l'égard de deux phases (stationnaire et mobile). L'échantillon est entraîné par la phase mobile au travers de la phase stationnaire qui a tendance à retenir plus ou moins les composés de l'échantillon à l'aide de différentes interactions. L'échantillon est adsorbé puis désorbé sur la phase stationnaire, ou est plus ou moins solubledans la phase mobile. 2 3Types de chromatographies
Type Critère de séparation
Adsorption Polarité
Partage Solubilité
Exclusion Taille des molécules
Échangeuse d'ions Charge ionique
Affinité Structure des protéines
Il est rare de pouvoir associer une méthode chromatographique à un seul phénomène. 4Types de chromatographies
Chromatographie
échangeuse d'ions
Chromatographie
d'exclusion 3 5Chromatographies d'adsorption
Phase mobile Nom
GazChromatographie en phase
vapeur (CPV) ou en phase gazeuse (GC)Liquide
Chromatographie couche mince
(CCMou TLC) ou éclairLiquide
Chromatographie liquide à haute
performance (CLHP ou HPLC) 6Utilité de la chromatographie
Selon la quantité de produit appliqué en chromatographie, on s'en sert pour: •Analyser< 1 mg de produit par CCM, HPLC ou CPV •Séparer ou purifierles produits d'une réaction par chromatographie éclair ou HPLC (50 mg à 15 g) •Doserdes produits. L'analyse quantitative se fait avec un étalon interne ou après préparation d'une courbe de calibration. 4 7Chromatographie d'adsorption: principe
La chromatographie d'adsorption est basée sur le partage des solutés entre l'adsorbant solide fixeet la phase mobile. Chacun des solutés est soumis à une force de rétention par adsorption et une force d'entraînement par la phase mobile. L'équilibre qui en résulte aboutit à une migration différentielle des solutés de l'échantillon à analyser, ce qui permet leur séparation. Les séparation sont basées sur le principe de polarité, c'est-à-dire l'existence de dipôles dans une structure moléculaire. Adsorbants possibles (du moins polaire au plus polaire): Papier, cellulose, amidon, carbonate de sodium, gel de silice, alumine, charbon activé. 8Adsorbants
Les adsorbants sont sous forme de granules
calibrés. La séparation est meilleure, mais plus lente si les grains sont fins.Plus un adsorbant est actif, plus il retient
fortement les composés polaires. La séparation se fait par ordre croissant de leurs forces d'interaction avec les composés polaires. 5 9Polarité des groupements
fonctionnels neutresLe gel de silice est polaire, il
a par conséquence une plus grande affinité pour les composés polaires:Un composé peu polaire
est peu adsorbé.Un composé polaire est
très adsorbé. R-H R-X R-NO 2RORROR
O RR O RH O RNR 2 O ROH O R-NH 2R-OH Ar-OH
Polarité croissante
Les molécules chargées ne migreront habituellement pas sur gel de silice, elles sont trop polaires. 10Phase mobile
Une phase mobile liquide est appelée éluant.C'est elle qui fait migrer les composés, son
choix est donc important. Il faut que le soluté soit solubledans l'éluant.Il est possible de faire des mélanges de
solvants pour changer sa polarité.Polarité croissante
Hexanes
CCl 4Benzène, Toluène
Et 2 O CH 2 Cl 2 AcOEtMeOH, EtOH
AcOH 6 11 Deux facteurs interviennent lors de l'interaction entre l'éluantet le soluté (mélange de composés à séparer): •la solubilité: on doit être en mesure de dissoudre le soluté dans l'éluant pour que la migration se fasse. •la polaritéde l'éluant va déterminer à quelle vitesse le composé migre. Moins un composé est polaire, moins il s'accroche à l'adsorbant, plus il migre avec l'éluant.Choix d'un éluant peu polaire Plus un composé est polaire, plus il s'accroche à l'adsorbant, moins il migre avec l'éluant. Choix d'un éluant polaireChoix de l'éluant
12Chromatographie sur couche mince
L'adsorbant (silice, 250 m d'épaisseur) est fixé sur une plaque (Al, verre) commercialement disponible. Le produit/mélange de produits est déposé sur la plaque à l'aide d'un capillaire. Les produits sont révélés après élution. 7 13Préparation d'un capillaire
Au laboratoire, les capillaires sont préparés au départ de pipettes Pasteur: • Chauffer la partie centrale de la pipette dans la flamme d'une torche au propane en tournant le tube jusqu'à ce qu'il soit mou. • Retirer de la flamme et étirer la pipette. • Laisser refroidir et couper la partie fine du milieu. 14Utilité des CCM
1.CCM analytiques(250 m, 2.5 x 7.5 cm)
• Vérifier la pureté d'un produit, quelques microgrammes suffisent • Suivre l'avancement d'une réaction • Vérifier l'efficacité d'une extraction liquide-liquide • Déterminer l'éluant pour la chromatographie éclair sur gel de silice2. CCM préparatives(1000
m, 20 x 20 cm) • Purification de petites quantités de produit (jusqu'à ~100 mg sur une plaque de 20 x 20 cm). La bande qui contient le produit purifié est grattée, puis la silice est extraite avec un solvant. 8 15Préparation de la CCM
ABC1. On trace un trait à ~1 cm du bord inférieur de la plaque.
On marque les futur dépôts, espacés d'environ 0.5 cm.On identifie chaque produit qu'on fera éluer.
2. Le produit/mélange doit toujoursêtre dilué dans
un solvant (Et 2 O, CH 2 Cl 2 , AcOEt...) assez volatil. Dans un vial, déposer 1 goutte ou 2-3 cristaux de produit + ~0.5 mL solvant. 16Élution de la CCM
3. On utilise un capillaire pour déposer le produit sur la
plaque puis on laisse évaporer le solvant. On peut spotter2-3 fois si l'échantillon est très dilué.
4. Élution: préparer une cuve d'élutionavec
•Bécher de 250 mL avec un papier absorbant à l'intérieur •Verre de montre Y verser 10 mL d'éluant (ex. 8 mL Hex + 2 mL AcOEt) Placer la CCM dans la cuve en veillant à ce que la ligne soit au-dessus du liquide. Faire éluer jusqu'à ~5 mm du bord et tracer un trait pour marquer le front de solvant. 9 17Révélation de la CCM
•À l'oeil nu: si le produit est coloré •À la lampe UV: les molécules qui absorbent les UV à 254 nm seront visibles (noyaux aromatiques par exemple). •Avec un révélateur chimique:l'iode est le premier révélateur à tester, car il est non destructif. Il permet de révéler des doubles liaisons et les halogénures. L'iode est évaporé à chaud ou dans la hotte.De nombreux autres existent: KMnO
4 , acide phosphomolybdique, vanilline, ninhydrine...UV KMnO
4 18Mesure du R
fProduit moins polaire, moins accroché
Produit plus polaire, plus accroché
1et 0 entrevaleur solvantdefront du Hauteur migration deHauteur Rf
Le R f (rapport frontal ou rétention frontale) est caractéristique d'un produit dans un éluant donné et pour une phase stationnaire donnée. Ll 1 l 2 10 19Influence de l'éluant
Lorsque la polarité du solvant augmente, le R
f augmente. Le R f augmente, puis diminue. Pour faire une séparation de deux produits par chromatographie, on cherche un éluant qui donne le plus grand R f possible, avec un R f pour le produit le moins polaire autour de 0,3.Polarité de l'éluant
100% Hexane 95% Hexane5% AcOEt90%Hexane10% AcOEt80%Hexane20% AcOEt70% Hexane30% AcOEt
20CCM bidirectionnelles
C'est une expérience qui permet de prouver si un produit décompose sur la silice, ou si un "spot" de la CCM contient en fait deux produits.Si élué dans un autre solvant
quotesdbs_dbs23.pdfusesText_29[PDF] chromatographie sur colonne
[PDF] avantages inconvénients chromatographie ionique
[PDF] electrophorese
[PDF] chromatographie d'exclusion
[PDF] chromatographie d'exclusion stérique polymère
[PDF] chromatographie gel filtration
[PDF] chromatographie d'exclusion stérique exercice
[PDF] chromatographie dexclusion exercice corrigé
[PDF] volume hydrodynamique
[PDF] chromatographie par perméation de gel (gpc)
[PDF] exercice chromatographie corrigé pdf
[PDF] qcm sur la chromatographie
[PDF] qcm chromatographie chimie analytique
[PDF] qcm chromatographie phase gazeuse
