 La réaction doxydoréduction
La réaction doxydoréduction
Les halogènes (F2; I2; Cl2;. O2) sont de puissants oxydants. 1.5)Etablir la demi-équation d'un couple. On étudie dans cet exemple le couple MnO4.
 Correction de lexercice « Encre sympathique »
Correction de lexercice « Encre sympathique »
C'est l'oxydant du couple I2(aq) / I-(aq). L'acide ascorbique présent dans le b) (4 pts) Demi-équations d'oxydoréduction : )(2. 2)(. 2. aqI e. aqI. −. − = +.
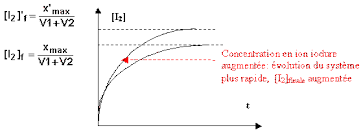 cinétique de réaction du diiode oxydoréduction
cinétique de réaction du diiode oxydoréduction
On fait la somme des 2 demi-équations pour obtenir l'équation bilan. 4 x (Cr2O7. 2-+ Equation bilan : 2 Fe3+ + 2 I- → 2 Fe2+ + I2. Seconde équation : 1/2 ...
 Les réactions doxydo-réduction
Les réactions doxydo-réduction
➔ Pour s'entraîner : « TS oxydoréduction demi équation ». 4/ Les réactions d'oxydoréduction. ➔ Le réducteur d'un couple (noté 1) peut participer à une
 CORRIGÉ
CORRIGÉ
1 août 2020 (1) et (2). C'est la même demi-équation pour le couple I2/I- qui intervient : ... 10- Écrire les demi-équations redox dans lesquelles ...
 Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Méthode : cas du couple Cr2O72-/Cr3 Applications Corrections
Ecrire les demi-équations relatives aux couples Redox suivants : Cu2+/Cu. Fe2+/Fe. S4O6. 2–/S2O3. 2–. I2/I–. MnO4. –/Mn2+. O2/H2O2. Ag+/Ag. Fe3+/Fe. Corrections.
 école numérique - thème : oxydoréduction titre de la leçon : couples
école numérique - thème : oxydoréduction titre de la leçon : couples
L-1 en milieu acide. 1. Écris les demi- équations électroniques et l'équation- bilan. 2. Calcule la concentration en diiode I2 et en ions
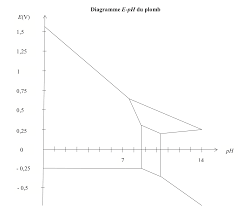
 Chapitre 5 : diagrammes potentiel-pH (E-pH) et potentiel-pL
Chapitre 5 : diagrammes potentiel-pH (E-pH) et potentiel-pL
Oxydoréduction (entre des espèces de n.o. différents). Ecriture de la demi-équation rédox utilisation de la formule de. Nernst puis de la convention de
 Loxydoréduction
Loxydoréduction
La demi-équation est écrite pour les deux membres d'un même couple Ox / Red + 5.I2 + 16.HO- à gauche H+ + HO- donne H2O : 2.MnO4. - +16.H2O +10.I-. 2Mn.
 La réaction doxydoréduction
La réaction doxydoréduction
Soit le couple I2/I- (diiode/ion iodure) établir la demi-équation de ce couple : qui cède des électrons et l'oxydant d'un autre couple redox qui les.
 Correction de lexercice « Encre sympathique »
Correction de lexercice « Encre sympathique »
a) (1 pt) Le diiode I2 de couleur brune en solution aqueuse
 CORRIGÉ
CORRIGÉ
1 août 2020 C'est la même demi-équation pour le couple I2/I- qui intervient : ... 10- Écrire les demi-équations redox dans lesquelles interviennent les ...
 Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
Exercice 29 p 131 : a) Équation de la réaction : Oxydation de S2O3
b) Il s'agit d'une réaction d'oxydoréduction car il a un échange d'électrons entre deux espèces (I2 l'oxydant et S2O3. 2- le réducteur). c) Volume de solution
 CM80 : Examen final — corrigé 1 Aspartame et neotame (667pts)
CM80 : Examen final — corrigé 1 Aspartame et neotame (667pts)
couple I2/I– : n.o. (I/I2) = 0 ; n.o. (I/I– ) = -I. D'où la demi-équation redox : I2 + 2e– = 2I– . — couple RCHO/RCO2. – : n.o. (C/RCHO) = +I ; n.o. (C/RCO2.
 cinétique de réaction du diiode oxydoréduction
cinétique de réaction du diiode oxydoréduction
On multiplie la demi-équation d'oxydation par le nombre d'électrons intervenant dans la demi- Equation bilan : 2 Fe3+ + 2 I- ? 2 Fe2+ + I2.
 LES THIOLS.pdf
LES THIOLS.pdf
L'équation bilan s'écrit : Les couples oxydant /réducteur présents sont : - Diiode / ion iodure : I2 / I-. Demi équation : I2 + 2 e- = 2I- (1).
 école numérique - thème : oxydoréduction titre de la leçon : couples
école numérique - thème : oxydoréduction titre de la leçon : couples
captant des électrons selon la demi-équation électronique : est un réducteur et ils forment le couple redox ... On donne les couples redox I2 I?.
 Les réactions doxydo-réduction
Les réactions doxydo-réduction
On décrit cette double possibilité par une « demi-équation » électronique : oxydant + n e- Pour s'entraîner : « TS oxydoréduction demi équation ».
 Loxydoréduction
Loxydoréduction
2) Établir l'équation en milieu acide
 Lecture 11 Redox Chemistry - Stanford University
Lecture 11 Redox Chemistry - Stanford University
Redox reactions are written as half-reactions which are in the form of reductions (which means an element is transformed from a higher oxidation state (e g +II) to a lower oxidation state (e g +I)): Ox + ne- = Red; Where the more oxidized form of an element is on the left and the reduced form is on the right n is the number of electrons
 7014 Redox Chemistry Handout - Massachusetts Institute of
7014 Redox Chemistry Handout - Massachusetts Institute of
There are three ways to represent a redox reaction; these are shown below with a representative biological redox reaction: acetaldehyde + NADH + H + ethanol + NAD + (1) Overall Reaction: (2) Electron-transfer diagram: acetaldehyde NADH + H + e-NAD + ethanol (3) Half-reactions: acetaldehyde + 2 H + + 2 e-ethanol + NADH NAD + + H + + 2 e-
 Balancing REDOX Reactions: Learn and Practice
Balancing REDOX Reactions: Learn and Practice
Apr 17 2013 · Here the equation is already written in an ionic equation format so we must do some more work to assign oxidation numbers (see ebook rules) ClO3¯ (aq) + I2 (s) à IO3¯ (aq) + Cl¯(aq) Oxidation Numbers: +5 -2 0 à +5 -2 -1 Yes the Iodine (I) has been oxidized and the Chlorine (Cl) has been reduced
 Oxidation- Reduction Chemistry - WRUV
Oxidation- Reduction Chemistry - WRUV
Half-Reactions ØConsider each process indivually: Oxidation Cu (s) ? Cu2+ (aq) + 2 e-Reduction [Ag+ + e-? Ag (s) ] x 2 Overall: Cu (s) + 2Ag+ (aq) ? Cu2+ (aq) + 2Ag (s) Oxidized (reducing agent) Reduced (oxidizing agent) 4 Balancing Redox Reactions Ø The Half-Reaction Method Three Steps: 1 Determine net ionic equations for both half
 Searches related to demi equation redox i2/i PDF
Searches related to demi equation redox i2/i PDF
During a REDOX reaction electrons are transferred directly from the reducer to the oxidizer with no separation of the two reactions • If we were able to isolate the half reactions into separate containers and connected the two containers electrically using platinum wire electrodes and a volt meter we could then measure that potential •
What are half-equations in a redox reaction?
These two equations are described as "eelectron-half-equations," "half-equations," or "ionic-half-equations," or "half-reactions." Every redox reaction is made up of two half-reactions: in one, electrons are lost (an oxidation process); in the other, those electrons are gained (a reduction process).
How do you determine the direction of a redox reaction?
Note: to determine the direction of a redox reaction, you do not need to use the Nernst equation. You only need to know the sign of ?E'?. you must reverse the sign of E'? for a reaction if you reverse the direction of the reaction. Here reaction (2) must be reversed.
What is a redox reaction?
Redox reactions are a major determinant of chemical species present in natural environments. Znº - 2e- Zn2+ (an oxidation half reaction, electrons lost) Cu2++ 2e- Cuº (a reduction half-reaction, electrons gained) The two species comprising half-reactions (e.g. Znº & Zn2+) are referred to as a “couple”.
Can a redox titration be applied to a mixture of analytes?
As with acid–base titrations, we can extend a redox titration to the analysis of a mixture of analytes if there is a significant difference in their oxidation or reduction potentials. Figure 9.42 shows an example of the titration curve for a mixture of Fe 2+ and Sn 2+ using Ce 4+ as the titrant.

CM80 : Examen final - corrigé
Rappel : Il fallait résoudre au choix 3 des 4 exercices proposés. Le total du barême indiqué
ici est donc de 26,68 points, mais l"examen est bien noté sur 20.1 Aspartame et neotame (6,67pts)
1.1 La molécule d"aspartame
1. Les atomes de carbone asymétrique sont indiqués ci-dessous (C*) :
H 2N C CO 2HO NHC C 6H 5OO2. L"énantiomère de l"aspartame a la formule suivante en représentation de Cram :
H 2N C CO 2HO NHC C 6H 5OO3. Les diastéréoisomères de l"aspartame ont les formules suivantes :
H 2N CO 2HO NHC 6H 5OOH 2N CO 2HO NHC 6H 5OO4. Puisque seul l"aspartame a un goût sucré, au contraire de ses stéréoisomères, on peut
en déduire que les récepteurs de goût sucré sont chiraux.1.2 Neotame vs aspartame
D"après les formules topologiues de la phénylalanine, de l"aspartame et du neotame : ni l"aspartame ni le néotame ne "con tient"de phén ylalanine(au plus elles con tiennent des groupement y ressemblant, mais cela a à voir avec les propositions (B) et (C)) : (A) est fausse; ils p ossèdenenttous deux u ngroup ementp ouvantformer de la phén ylalaninelors de l"hydrolyse : (B) est fausse; par élimination il reste la prop osition(C) : "dans les conditions biologiques de la digestion, l"hydrolyse du neotame ne produit pas de phénylalanine". 11.3 Synthèse du neotame
1. D"après la formule topologique du meotame et d"après les données, les liaisons indiquées
en gris peuvent être formées en faisant réagir les molécules suivantes : (A)Cl (B)HO ONH 2O NHC 6H 5OOH (C)H 3COH Les sous-produits de cette synthèse sont HCl et H 2O.2. Alternativement (ou dans le même processus) on peut produire le neotame (ou le réactif
(B) ci-dessus) par synthèse peptidique :Réactifs : HO
ONH 2O OHetH 2NC 6H 5OOHProtection : GP
1ONH P 2GO OHetH 2NC 6H 5OGP3-Liaison p eptidique: GP
1ONH P 2GO NHC 6H 5OGP3-Déprotection : HO
ONH 2O NHC 6H 5OOH 22 Variations sur le glucose (6,67pts)
2.1 Photosynthèse
1. a) Couple O
2/H2O : n.o. (O/O2) = 0; n.o. (O/H2O) = -II.
D"où la demi-équation redox : O
2+ 4e-4H+= 2H2O
1. b) Couple CO
2/C6H12O6: n.o. (C/CO2) = +IV; n.o. (C/C6H12O6) = 0.
D"où la demi-équation redox : CO
2+ 4e-4H+=16
C6H12O6+ H2O
2. Voici l"équation de l"oxydation du glucose lors de la respiration :
16C6H12O6+ O2!CO2+ H2O
3. Lors de la respiration, la matière organique (i.e. le glucose, contenant de l"hydrogène et
du carbone) est oxydée en dioxyde de carbone : une matière inorganique car ne contenant pas d"hydrogène.4. La photosynthèse est la réaction inverse de la respiration : respectivement, oxydation
du glucose et réduction du dioxyde de carbone. Or, la respiration est une transformation spontanée. Donc, la photosynthèse est une transformation forcée.5. Un accumulateur est le siège :
d"une réaction sp ontanéelors de la déc harge; d"une réaction forcée l orsde la c harge: un générate urexterne doit fournir de l"énergie à l"accumulateur.Une cellule photosynthétique est le siège :
d"une réaction sp ontanéelors de la respiration : "déc harge"fournissan tde l"énergieà la cellule sous forme d"ATP;
d"une réaction forcée lors de la photosyn thèse: "c harge"de la cellule p ermisepar l"énergie lumineuse fournie, transformée en ATP.2.2 Sucre inverti
1. Le glucose et le fructose sont deux molécules différentes ayant la même formule brute :
ce sont des isomères.2. D"après les formules brutes, l"autre réactif est l"eau (d"où le nom d" "hydrolyse" donné
à la réaction) :
C12H22O11+ H2O!C6H12O6(glucose) + C6H12O6(fructose)
3. La concentration initiale en saccharose est de [S]
0= 0,2 molL-1dans les trois expé-
riences. Le temps de demi-réactiont1=2est donc tel que[S]t1=2= 0;1mol:L1: a vecune concen tration0;5cde catalyseur :t1=2= 0;6s; a vecune concen trationcde catalyseur :t1=2= 0;3s; a vecune concen tration2cde catalyseur :t1=2= 0;15s; La réaction est donc d"autant plus rapide que la concentration de catalyseur est élevée. Le temps de demi-réaction (et donc la vitesse de réaction) est inversement proportionnel à la concentration en catalyseur (dans la plage où les mesuresont été effectuées).4. D"après la courbe obtenue pour une concentration en catalyseur de0;5c, la décroissance
de [S] est linéaire en temps : la réaction est donc d"ordre courant zéro par-rapport au saccharose.Remarque :il est bien possible que cela soit une dégénérescence d"ordre due aux conditions expérimentales. 3 Remarque 2 :l"allure des autres courbes faisant penser à une exponentielle, la réponse "ordre 1" était aussi acceptée.3 Dosage du glucose libre d"un jus de fruit (6,67pts)
3.1 Mélange initial
La quantité de diiode initialement introduit dans le mélange vaut : nD=V0c0
Application numérique :nD= 4;0:104mol.
3.2 Réaction entre le glucose et le diiode
1. Les couples redox en présence sont les suivants :
couple I2/I-: n.o. (I/I2) = 0; n.o. (I/I-) = -I.
D"où la demi-équation redox : I
2+ 2e-= 2I-.
couple R CHO/RCO2-: n.o. (C/RCHO) = +I; n.o. (C/RCO2-) = +III.
D"où la demi-équation redox : RCO
2-+ 2e-+ 2H2O = RCHO + 3HO-(en
milieu basique). On obtient donc bien l"équation bilan indiquée : I2+ RCHO + 3HO-!2I-+ RCO2-+ 2H2O
2. Après l"arrêt de la réaction (épuisement du réactif limitant) la solution reste colorée :
il reste donc du diiode. Le réactif limitant est donc le glucose.3. Tableau d"avancement de la réaction :AvancementI
2+ RCHO + 3HO-!2I-+ RCO2-+ 2H2O0n
DnGexcès00excès
xn DxnGxexcès2xxexcès
x maxnDxmaxn
Gxmax= 0excès2xmaxx
maxexcès4. On notenRla quantité de diiode n"ayant pas réagi :nR=nDxmax.
Or,nGxmax= 0(réactif limitant). On obtient donc :nG=xmax=nDnR.3.3 Dosage du diiode en excès
1. D"après la courbe d"étalonnage spectrophotométrique, la concentration du diiode res-
tant vaut : [I2]R= 3,0.10-3molL-1(pour une absorbanceA= 1;5).
2. La quantité de diiode restant dans le mélange réactionnel vaut donc :
nR= [I2]RVfiole
Application numérique :nR= 1;5:104mol.
La quantité de glucose initialement présente vaut : nG=nDnR
4Application numérique :nG= 2;5:104mol.
3. La quantité de glucose présent dans un litre de jus de fruits vaut donc :
n0G=nGV
fioleApplication numérique :n0G= 0;125mol.
La masse de glucose présent dans un litre de jus de fruit vaut : mG=n0GM
Application numérique :mG= 22;5g.
4 Dioxyde de soufre (6,67pts)
a) Couple (SO42-/SO2) : n.o. (S/SO42-) = +VI; n.o. (S/SO2) = +IV.
D"où la demi-équation redox : SO
42-+ 2e-4H+= SO22H2O.
Couple (MnO
4-/Mn2+) : n.o. (Mn/MnO4-) = +VII; n.o. (Mn/Mn2+) = +II.
D"où la demi-équation redox : MnO
4-+ 5e-8H+= Mn2+4H2O.
L"équation de la réaction entre le dioxyde de soufre et le permanganate s"écrit donc : 2MnO4-+ 5SO2+ 2H2O!2Mn2++ 5SO42-+ 4H+
b) À l"équivalence du titrage, les réactifs MnO4-et SO2ont été introduits en quantités
stoechiométriques. c) On a donc à l"équivalence la relation : n 15 =ne2 d) À l"équivalence :n15 =ne2 ssi C1V15 =cVe2 ssic1=5cVe2V1Application numérique :c1= 2;0:102mol:L1.
e) La massem1de SO2contenue dans 1 litre de solutionSvaut donc : m1=c1MSO2
Application numérique :m1= 1;28g:L1(MSO2= 64g:mol1). f) La massem2de SO2contenue dans un mètre cube d"air est donnée par la dilution initiale de l"air pollué dans la solutionS: m 2=m1V 0V airApplication numérique :m2= 1;28:104g:m3.
g) Conversion d"unités :m2= 128g:m3. Le seuil d"alerte n"est donc pas atteint. 5quotesdbs_dbs29.pdfusesText_35[PDF] potentiel standard cl2/cl-
[PDF] clo-/cl-
[PDF] couple redox clo-/cl-
[PDF] demi equation clo-/cl-
[PDF] hclo/cl2
[PDF] demi equation redox sn2+/sn
[PDF] couple redox dichlore
[PDF] claforan iv
[PDF] claforan dilution
[PDF] claforan posologie
[PDF] claforan per os
[PDF] claforan cp
[PDF] claforan dci
[PDF] claforan 1g
