 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Liqueur de Fehling. Solution 1. CuSO4 5H2O. 40 g. Eau. 300 mL. (prévoir un excès de 5-10% de CuSO4). Solution 2. NaOH. 130 g. Tartrate de K et Na. 160 g. Eau.
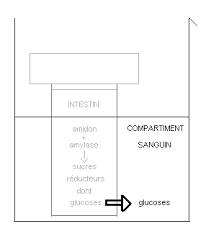 Kit dialyse
Kit dialyse
sucres réducteurs à l'aide de réactions au lugol et à la liqueur de Fehling A + B. L'autre groupe réalise la digestion In Vitro en mettant de l'amidon en ...
 Sans titre
Sans titre
Ces oses se comportent comme des réducteurs : ils réduisent la liqueur de Fehling à C'est un sucre réducteur. ◗. Le lactose formé d'une molécule de glucose ...
 CODE: SVT DURÉE : 6H
CODE: SVT DURÉE : 6H
Le sucre réducteur du pain est le glucose et le sucre réducteur du lait est le lactose. La liqueur de Fehling qui permet de caractériser les sucres réducteurs
 Fiche technique dutilisation de réactifs spécifiques de différents
Fiche technique dutilisation de réactifs spécifiques de différents
- Verser ........ mL de la solution dans un tube à essais
 Observations sur la méthode de Gabriel Bertrand pour le dosage
Observations sur la méthode de Gabriel Bertrand pour le dosage
8 oct. 2019 comme officielle qui consiste à oxyder le sucre réducteur au moyen d'une liqueur du type Barreswill-Fehling
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
déduire la quantité d'oses réducteurs totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Test à la liqueur de Fehling : mise en évidence des sucres réducteurs. La liqueur de Fehling est une solution renfermant des ions Cu2+ de couleur bleue en
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling. Le document 1 nous rappelle que la présence de sucres réducteurs (glucose et maltose) traduit l'hydrolyse des polysaccharides. On en ...
 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Pour une même quantité de solution de liqueur de Fehling utilisée soit 5 mL
 Sans titre
Sans titre
C'est le sucre de table ou sucre blanc. Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling.
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur de la solution à.
 Kit dialyse
Kit dialyse
Réactif. Couleur. LUGOL. LIQUEUR DE FEHLING A + B. Chauffée au bain-marie. Du réactif. Avec ajout de sucres réducteurs. Avec ajout d'amidon
 TP 2 : De lamidon au maltose une simplification moléculaire Mise
TP 2 : De lamidon au maltose une simplification moléculaire Mise
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL) à température ambiante.
 1 L A 04 Les glucides B version prof
1 L A 04 Les glucides B version prof
Dans un tube à essai contenant de la liqueur de Fehling de couleur bleue L'acide chlorhydrique transforme le saccharose en sucres réducteurs : glucose ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Biochimie : liqueur de Fehling lugol
 Atelier de biologie mise en évidence de glucides
Atelier de biologie mise en évidence de glucides
présence de différents sucres dans les aliments. Durée de l'activité. 1 séance indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling.
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL). - eau distillée.
 MÉMOIRE DE MASTER
MÉMOIRE DE MASTER
Dosage des sucres réducteurs. A) Principe. Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs.
 [PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
[PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
Liqueur de Fehling Solution 1 CuSO4 5H2O 40 g Eau 300 mL (prévoir un excès de 5-10 de CuSO4) Solution 2 NaOH 130 g Tartrate de K et Na 160 g Eau
 Dosage des sucres réducteurs par la méthode de Fehling
Dosage des sucres réducteurs par la méthode de Fehling
Cette méthode de dosage repose sur la réduction de la liqueur de Fehling mélange d'une solution de sulfate de cuivre et de sel de Seignette en présence de
 Des sucres réducteurs - Mettre en évidence - Académie de Versailles
Des sucres réducteurs - Mettre en évidence - Académie de Versailles
La liqueur de Fehling renferme des ions cuivre II de couleur bleue A chaud en présence d'un réducteur se forme un précipité rouge brique d'oxyde de cuivre
 [PDF] Fiche technique dutilisation de réactifs spécifiques de différents
[PDF] Fiche technique dutilisation de réactifs spécifiques de différents
A chaud et en présence de glucides réducteurs la liqueur de Fehling donne un précipité rouge brique d'oxyde de cuivre Cu2O A : Couleur initial du réactif ;
 [PDF] MÉMOIRE DE MASTER - University of Biskra Repository
[PDF] MÉMOIRE DE MASTER - University of Biskra Repository
Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs contenus dans l'échantillon (Audigier et al 1984) 3 3 1 10
 [PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
[PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
Elle permet aussi de présenter aux jeunes deux indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling Remarque : Cette expérience est très prisée
 [PDF] Les molécules organiques
[PDF] Les molécules organiques
C'est le sucre de table ou sucre blanc Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling
 [PDF] Chimie des sucrespdf - ORBi
[PDF] Chimie des sucrespdf - ORBi
Les OSES encore appelés monosaccharides ou sucres simples sont les plus simples des glucides Ils sont REDUCTEURS Les sures simples sont des chaînes carbonées
 [PDF] 1 L A 04 Les glucides B version prof
[PDF] 1 L A 04 Les glucides B version prof
Interprétation : certains sucres comme le glucose réagissent avec la liqueur de Fehling ; ils sont appelés "sucres réducteurs"
 [PDF] TP 21 : Dosage du glucose
[PDF] TP 21 : Dosage du glucose
Le glucose réagit à chaud avec la liqueur de Fehling La transformation est visualisée par un changement de couleur : la teinte du mélange vire du bleu au
Pourquoi le glucose réagit avec la liqueur de Fehling ?
La raison est que le saccharose s'hydrolyse en fructose et en glucose, et que ce dernier réagit avec les ions cuivre(II) de la liqueur.Pourquoi le sucre est réducteur ?
Les sucres réducteurs sont des sucres simples donneurs d'électrons dans une réaction d'oxydo-réduction. Par exemple le glucose, le fructose et le maltose. Ils poss?nt une fonction aldéhyde. Les sucres non réducteurs ne poss?nt pas cette fonction aldéhyde.Comment mettre en évidence le sucre réducteur ?
Mettre la substance à tester en solution dans un tube à essai avec de l'eau distillée. Faire chauffer au bec bunsen ou mieux mettre au bain-marie à 100°C quelques minutes. La formation d'un précipité rouge brique indique la présence de sucres réducteurs.- On utilise la liqueur de Fehling pour caractériser les aldéhydes aliphatiques (la réaction est moins nette pour les aldéhydes aromatiques), tel le glucose. La réaction provoque la formation d'un précipité d'oxyde cuivreux rouge-brun. On l'utilise aussi pour déterminer la proportion de sucres réducteurs.
Mise en situation et recherche à mener
Notre organisme satisfait ses besoins en glucose en particulier grâce à son alimentation riche en amidon. Cette molécule est essentiellement apportée par les
féculents, tels que les céréales, les pommes de terre ou différents représentants de la famille des légumineuses. Or les molécules d'amidon ont une taille rendant
impossible leur absorption au niveau de l'intestin et donc leur arrivée dans le sang.On cherche à montrer, in vitro, que la digestion enzymatique des molécules d'amidon se réalise dans les conditions correspondant à celles qui règnent
dans le corps humain.Ressources
Document 1 : la digestion de l'amidon par l'amylase pancréatique L'amylase pancréatique est une enzyme sécrétée par le pancréas qui provoque la rupture de certaines liaisons chimiques entre les molécules de glucose.Cette enzyme agit en particulier sur l'amidon.
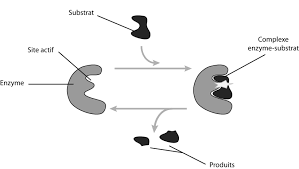
Document 2 : l'activité enzymatique
Les enzymes sont des molécules protéiques complexes dont l'activité dépend des conditions du milieu : température, acidité. Elles servent de catalyseurs car ellesrendent possibles ou accélèrent grandement les réactions chimiques vitales.Document 3 : Tableau des réactifs de certains glucides
Le tableau ci-dessous indique pour différentes molécules et différents réactifs utilisés, les résultats obtenus. Par exemple, l'utilisation du réactif " eau iodée » permet de révéler la présence d'amidon par une coloration violet-noir. En revanche, l'eau iodée ne permet pas de révéler la présence de maltose (dans ce cas, la coloration reste jaune). Etape A1 : Concevoir une stratégie pour résoudre une situation-problèmeProposer une démarche d'investigation permettant de montrer, in vitro, que la digestion enzymatique des molécules d'amidon se réalise dans les conditions
correspondant à celles qui règnent dans le corps humain. Rédiger votre proposition sur votre copie(D'après http://www.cnrs.fr) Partie 2 - Glycémie et diabèteTS Spécialité SVT Etape A2 : Mettre en oeuvre un protocole de résolution pour obtenir des résultats exploitablesUtiliser le matériel fourni pour mettre en évidence les conditions de la simplification moléculaire de l'amidon.
Matériel à utiliser :
-12 tubes à essais -3 pipettes avec petit bécher (pour rinçage des pipettes) ; eau distillée -1 plateau de coloration = plaques à cupules + feutres pour marquage -bain-marie 37° -bain-marie 70° - bac à glace -eau iodée (réactif spécifique de l'amidon) -liqueur de Fehling (réactif spécifique des sucres réducteurs, comme le maltose) -solution d'amylase (+ pipette 5 mL) à température ambiante -solution d'amylase (+ pipette 5 mL) à température froide -solution d'empois d'amidon (+ pipette 10 mL) à température ambiante- solution d'empois d'amidon (+ pipette 10 mL) à température froideTests à réaliser toutes les 15 minutes
Test 1 : présence d'amidon : bien mélanger le contenu du tube, puis prélever 1 goutte de la solution à tester et la déposer dans un des puits de la plaque. Rajouter de l'eau iodée. Une coloration violet-noir indique la présence d'amidon. Test 2 : présence de sucres réducteurs (ex : glucose, maltose) : bien mélanger le contenu du tube, puis prélever environ 2 mL de la solution à tester et la verser dans un tube à essai ; rajouter 1 mL de liqueur de Fehling (le contenu d'un prélèvement). Faire chauffer ce tube en le déposant dans le bain-marie à 70°C. Un précipité rouge-brique indique la présence de sucres réducteurs, comme le maltose.Réalisation du protocole :
1. Préparer 3 tubes à essai :
- tube 1 : 10 mL de solution d'amidon tempérée + 3 mL d'eau distillée - tube 2 : 10 mL de solution d'amidon tempérée + 3 mL d'amylase tempérée - tube 3 : 10 mL de solution d'amidon froide + 3 mL d'amylase froidePenser à repérer vos tubes
2. Placer les tubes 1 et 2 au bain-marie à 37°C et le tube 3 dans le bac à glace.
3. Pour chacun des 3 tubes, réaliser les deux tests suivants : test 1 : présence d'amidon - test 2 : présence de sucres réducteurs
Ces deux tests doivent être réalisés toutes les 15 minutes, donc à t=0, t=15 min et t=30 min.
Attention de bien mélanger le contenu des tubes avant les prélèvements et de rincer vos pipettes entre les prélèvements!!!
Etape B - Communiquer et exploiter les résultats pour répondre au problème (durée : environ 20 minutes)
-Sous la forme la plus pertinente, présenter les résultats pour mettre en valeur les informations utiles à la résolution du problème.
-Exploiter les résultats obtenus afin de répondre au problème posé. Partie 2 - Glycémie et diabèteTS Spécialité SVTCorrection
A1. Proposer une démarche d'investigation permettant de montrer, in vitro, que la digestion enzymatique des molécules d'amidon se réalise dans les conditions
correspondant à celles qui règnent dans le corps humain.a. Nous cherchons à montrer que la digestion enzymatique se réalise dans des conditions correspondant à celles de l'organisme. Dans le cadre de cette activité, nous
nous limiterons aux seules conditions de température et nous chercherons donc à vérifier que la digestion enzymatique se réalise préférentiellement à 37°C,
température normale du corps humain.b. Pour cela, nous allons comparer les résultats d'une digestion enzymatique de l'amidon par l'amylase dans deux conditions de température différentes : à 37°C et à
faible température. Nous vérifierons également que l'amidon ne s'hydrolyse pas spontanément en préparant une solution dépourvue d'enzyme.
Pour vérifier l'hydrolyse de l'amidon, nous testerons : - la présence d'amidon avec un test à la liqueur de Fehling- la formation des sucres producteurs (issus de l'hydrolyse de l'amidon) avec un test à la liqueur de Fehling
c. Si la digestion enzymatique se réalise uniquement (ou préférentiellement) dans les conditions de l'organisme, nous devrions observer une diminution de la teneur en
amidon et une augmentation de la production de sucres réducteurs uniquement (ou préférentiellement) dans la solution " amidon + amylase » placée à 37°C. Dans les
deux autres solutions " amidon + amylase » à température froide et " amidon seul » à 37°C, la teneur en amidon devrait rester constante et aucun sucre réducteur ne
devrait être produit. B1Tableau de présentation des résultats expérimentauxTubesContenu des
tubesConditionsRésultats des tests à l'eau iodée et à la liqueur de Fehling (LF)T0T + 15 minutesT +30 minutes
Test eau iodéeTest LFTest eau iodéeTest LFTest eau iodéeTest LF1Amidon + eau
distillée37°Cprésence d'amidonpas de sucres réducteursprésence d'amidonpas de sucres réducteursprésence d'amidonpas de sucres réducteurs2Amidon +
amylase37°Cprésence d'amidonpas de sucres réducteursFaible présence d'amidonsucres réducteursPas d'amidonsucres réducteurs3Amidon +
amylasefroidesprésence d'amidonpas de sucres réducteursprésence d'amidonpas de sucres réducteursprésence d'amidonpas de sucres réducteursB2 : Exploitation
Nous n'observons la présence de sucres réducteurs et la disparition d'amidon que dans le tube 2, placé à 37°C. Dans les deux autres tubes, la quantité d'amidon est
constante au cours des 30 minutes de réaction et il n'y a pas de production de sucres réducteurs.
Nous savons que l'action de l'amylase se caractérise par une hydrolyse de l'amidon, donc une " disparition » de cette molécule et la production de sucres
réducteurs.Nous en déduisons donc que l'amylase n'a été active que dans le tube 2, donc uniquement à 37°C. Cela confirme bien que l'amylase agit très préférentiellement
dans les conditions de l'organisme. Partie 2 - Glycémie et diabèteTS Spécialité SVTMatériel labo
Matériel par poste
-12 tubes à essais -3 pipettes + petit bécher pour rinçage -1 plateau de coloration = plaques à cupules -bain-marie 37° + thermomètre (à partager entre 2 ou 3 postes) -bac à glace -bain-marie 80° + thermomètre (à partager entre 2 ou 3 postes) -chronomètre -eau iodée (réactif spécifique de l'amidon) -liqueur de Fehling (réactif spécifique des sucres réducteurs, comme le maltose) -eau distillée -feutre (pour tube)Matériel bureau
-solution d'amylase, avec pipette 5 mL à température ambiante -solution d'amylase, avec pipette 5 mL au froid !!! -solutions de maltose, avec pipette 5 mL-solution d'empois d'amidon tempérée (+ pipette 10 mL) : mettre deux béchers de 500 mL avec 1 pipette par bécher
-solution d'empois d'amidon froide (+ pipette 10 mL)quotesdbs_dbs5.pdfusesText_10[PDF] diholoside réducteur et non réducteur
[PDF] pouvoir réducteur des glucides
[PDF] le système hormonal
[PDF] glandes endocrines et hormones
[PDF] système endocrinien pour les nuls
[PDF] liste des hormones pdf
[PDF] type d'hormone
[PDF] les hormones et leurs fonctions pdf
[PDF] lipides simples et complexes
[PDF] classification des microorganismes ppt
[PDF] le monde microbien wikipedia
[PDF] tableau de classification des micro-organisme
[PDF] pfe pont dalle
[PDF] pont a poutre en béton armé pdf
