 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Liqueur de Fehling. Solution 1. CuSO4 5H2O. 40 g. Eau. 300 mL. (prévoir un excès de 5-10% de CuSO4). Solution 2. NaOH. 130 g. Tartrate de K et Na. 160 g. Eau.
 Kit dialyse
Kit dialyse
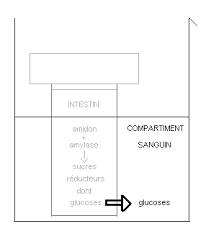
sucres réducteurs à l'aide de réactions au lugol et à la liqueur de Fehling A + B. L'autre groupe réalise la digestion In Vitro en mettant de l'amidon en ...
 Sans titre
Sans titre
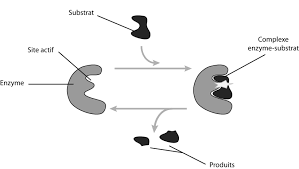
Ces oses se comportent comme des réducteurs : ils réduisent la liqueur de Fehling à C'est un sucre réducteur. ◗. Le lactose formé d'une molécule de glucose ...
 CODE: SVT DURÉE : 6H
CODE: SVT DURÉE : 6H
Le sucre réducteur du pain est le glucose et le sucre réducteur du lait est le lactose. La liqueur de Fehling qui permet de caractériser les sucres réducteurs
 Fiche technique dutilisation de réactifs spécifiques de différents
Fiche technique dutilisation de réactifs spécifiques de différents
- Verser ........ mL de la solution dans un tube à essais
 TP 2 : De lamidon au maltose une simplification moléculaire Mise
TP 2 : De lamidon au maltose une simplification moléculaire Mise
- liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL) à température ambiante. - solution d
 Observations sur la méthode de Gabriel Bertrand pour le dosage
Observations sur la méthode de Gabriel Bertrand pour le dosage
8 oct. 2019 comme officielle qui consiste à oxyder le sucre réducteur au moyen d'une liqueur du type Barreswill-Fehling
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
déduire la quantité d'oses réducteurs totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Test à la liqueur de Fehling : mise en évidence des sucres réducteurs. La liqueur de Fehling est une solution renfermant des ions Cu2+ de couleur bleue en
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling. Le document 1 nous rappelle que la présence de sucres réducteurs (glucose et maltose) traduit l'hydrolyse des polysaccharides. On en ...
 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Pour une même quantité de solution de liqueur de Fehling utilisée soit 5 mL
 Sans titre
Sans titre
C'est le sucre de table ou sucre blanc. Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling.
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur de la solution à.
 Kit dialyse
Kit dialyse
Réactif. Couleur. LUGOL. LIQUEUR DE FEHLING A + B. Chauffée au bain-marie. Du réactif. Avec ajout de sucres réducteurs. Avec ajout d'amidon
 TP 2 : De lamidon au maltose une simplification moléculaire Mise
TP 2 : De lamidon au maltose une simplification moléculaire Mise
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL) à température ambiante.
 1 L A 04 Les glucides B version prof
1 L A 04 Les glucides B version prof
Dans un tube à essai contenant de la liqueur de Fehling de couleur bleue L'acide chlorhydrique transforme le saccharose en sucres réducteurs : glucose ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Biochimie : liqueur de Fehling lugol
 Atelier de biologie mise en évidence de glucides
Atelier de biologie mise en évidence de glucides
présence de différents sucres dans les aliments. Durée de l'activité. 1 séance indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling.
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL). - eau distillée.
 MÉMOIRE DE MASTER
MÉMOIRE DE MASTER
Dosage des sucres réducteurs. A) Principe. Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs.
 [PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
[PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
Liqueur de Fehling Solution 1 CuSO4 5H2O 40 g Eau 300 mL (prévoir un excès de 5-10 de CuSO4) Solution 2 NaOH 130 g Tartrate de K et Na 160 g Eau
 Dosage des sucres réducteurs par la méthode de Fehling
Dosage des sucres réducteurs par la méthode de Fehling
Cette méthode de dosage repose sur la réduction de la liqueur de Fehling mélange d'une solution de sulfate de cuivre et de sel de Seignette en présence de
 Des sucres réducteurs - Mettre en évidence - Académie de Versailles
Des sucres réducteurs - Mettre en évidence - Académie de Versailles
La liqueur de Fehling renferme des ions cuivre II de couleur bleue A chaud en présence d'un réducteur se forme un précipité rouge brique d'oxyde de cuivre
 [PDF] Fiche technique dutilisation de réactifs spécifiques de différents
[PDF] Fiche technique dutilisation de réactifs spécifiques de différents
A chaud et en présence de glucides réducteurs la liqueur de Fehling donne un précipité rouge brique d'oxyde de cuivre Cu2O A : Couleur initial du réactif ;
 [PDF] MÉMOIRE DE MASTER - University of Biskra Repository
[PDF] MÉMOIRE DE MASTER - University of Biskra Repository
Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs contenus dans l'échantillon (Audigier et al 1984) 3 3 1 10
 [PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
[PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
Elle permet aussi de présenter aux jeunes deux indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling Remarque : Cette expérience est très prisée
 [PDF] Les molécules organiques
[PDF] Les molécules organiques
C'est le sucre de table ou sucre blanc Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling
 [PDF] Chimie des sucrespdf - ORBi
[PDF] Chimie des sucrespdf - ORBi
Les OSES encore appelés monosaccharides ou sucres simples sont les plus simples des glucides Ils sont REDUCTEURS Les sures simples sont des chaînes carbonées
 [PDF] 1 L A 04 Les glucides B version prof
[PDF] 1 L A 04 Les glucides B version prof
Interprétation : certains sucres comme le glucose réagissent avec la liqueur de Fehling ; ils sont appelés "sucres réducteurs"
 [PDF] TP 21 : Dosage du glucose
[PDF] TP 21 : Dosage du glucose
Le glucose réagit à chaud avec la liqueur de Fehling La transformation est visualisée par un changement de couleur : la teinte du mélange vire du bleu au
Pourquoi le glucose réagit avec la liqueur de Fehling ?
La raison est que le saccharose s'hydrolyse en fructose et en glucose, et que ce dernier réagit avec les ions cuivre(II) de la liqueur.Pourquoi le sucre est réducteur ?
Les sucres réducteurs sont des sucres simples donneurs d'électrons dans une réaction d'oxydo-réduction. Par exemple le glucose, le fructose et le maltose. Ils poss?nt une fonction aldéhyde. Les sucres non réducteurs ne poss?nt pas cette fonction aldéhyde.Comment mettre en évidence le sucre réducteur ?
Mettre la substance à tester en solution dans un tube à essai avec de l'eau distillée. Faire chauffer au bec bunsen ou mieux mettre au bain-marie à 100°C quelques minutes. La formation d'un précipité rouge brique indique la présence de sucres réducteurs.- On utilise la liqueur de Fehling pour caractériser les aldéhydes aliphatiques (la réaction est moins nette pour les aldéhydes aromatiques), tel le glucose. La réaction provoque la formation d'un précipité d'oxyde cuivreux rouge-brun. On l'utilise aussi pour déterminer la proportion de sucres réducteurs.
Remerciements
Biskra Université Mohamed Khider de
Faculté des sciences exactes et
vie sciences de la nature et de la la Département des sciences de nature et de la vieDomaine : Sciences de la nature et de la vie
Filière : Sciences biologiques
Spécialité : Biotechnologie et valorisation des plantesPrésenté et soutenu par :
Nadjat BERKEM Assia MANSOUL
Le : Mardi 9 juillet 2019
Thème
Contribution à l'étude des caractéristiques physico-chimiques et extraction des sucres de quelques variétés des dattes de ZibanJury :
Mme. HAMMIA MAA Université de Biskra Président M. Zayane LAIADHI MCA Université de Biskra Rapporteur Mme. BELKHARCHOUCHE MCB Université de Biskra ExaminateurM. Karim REKIS Chercheur Université de Biskra co-rapporteur
Année universitaire : 2018 - 2019
MÉMOIRE DE MASTER
Remerciements
Remerciments
avoir donné le courage et la santé pour achever ce travail Nos remercie très particuliers à notre encadreur Monsieur REKIS .K et liaidhi . Z , maitre de conférences, de Et toute ma reconnaissance à tous les enseignants du département biologique Un grand remerciement à tous ceux qui ont attribuée de près ou de loin à la réalisation de ce mémoireDédicac
Sommaire
Sommaire
Remerciments
Dédicac
Liste des tableaux ........................................................................................................................ I
Liste des figures ........................................................................................................................ II
Liste des abréviations ............................................................................................................... IV
Introduction générale .................................................................................................................. 1
PREMIERE PARTIE : PARTIE BIBLIOGRAPHIQUE
Chapitr 1. LE PALMIER DATTIER
1.1. Généralités sur le palmier dattier ................................................................................ 2
. Position systématique .................................................................................................... 2
1.3. Biologie du palmier dattier ........................................................................................... 3
1.3.1. La reproduction sexuée ............................................................................................. 3
1.3.2. La reproduction asexuée ........................................................................................... 3
1.3.2.1. Rejet ................................................................................................................... 3
1.3.2.2. Gourmand ou roukab .......................................................................................... 3
1.3.2.3. Culture in vitro ................................................................................................... 3
1.4. Morphologie du palmier dattier ................................................................................... 3
1.4.1. Organes végétatifs ..................................................................................................... 3
1.4.1.1. Le système racinaire ........................................................................................... 3
1.4.1.2. Le stipe ou tronc ................................................................................................. 3
1.4.1.3. Les feuille ........................................................................................................... 3
1.4.1.4. Les organes floraux ............................................................................................ 4
1.4.1.5. La fleur femelle .................................................................................................. 4
1.4.1.6. La fleur mâle ...................................................................................................... 4
Chapitre 2. LA DATTE
2.1. Description de la datte ................................................................................................... 6
2.2. Classification des dattes ................................................................................................ 6
2.2.1. Selon la consistance des dattes ................................................................................. 6
2.2.1.1 Les dattes molles ................................................................................................. 7
2.2.1.2 Les dattes demi- molles ....................................................................................... 7
2.2.1.3 Les dattes sèches ................................................................................................. 7
2.2.2.1. Dattes fines ou exportables : dont le type est représenté par la Deglet Nour. ....... 7
2.2.2.2. Dattes communes : représenté par Ghares ; Degla Beida ...................................... 7
2.3. Formation et maturation de la datte ............................................................................ 7
Sommaire
2.3.1. Stade Hababouk ........................................................................................................ 7
2.3.2. Stade Khalal .............................................................................................................. 7
2.3.3. Stade Bser ................................................................................................................. 7
2.3.4. Stade routab .............................................................................................................. 7
2.3.5. Stade tmar ................................................................................................................. 7
2.4. Composition biochimique ............................................................................................. 8
2.4.1. Partie comestible ....................................................................................................... 8
2.4.1.1 La pulpe de dattes ................................................................................................ 8
A. L'eau ........................................................................................................................ 8
B. Les sucre ................................................................................................................. 8
C. Les protéines .......................................................................................................... 8
D. Les fibres ................................................................................................................ 9
E. Eléments minéraux .................................................................................................. 9
F. Matières grasses ...................................................................................................... 9
G. Vitamines ................................................................................................................ 9
H. Enzymes .................................................................................................................. 9
I. Constituants mineurs ................................................................................................ 9
Pigments .............................................................................................................. 9
Polyphénols ..................................................................................................... 9
Tanins ................................................................................................................... 9
Flavones ............................................................................................................... 9
Les acides organiques. .......................................................................................... 9
Les composés volatils (Flaveur) ........................................................................... 9
2.4.2. De la partie non comestible "Noyau" ...................................................................... 10
2.5. Vérification et contrôle de qualité .............................................................................. 10
Deuxième PARTIE : PARTIE EXPERIMENTALE
Chapitre 3. MATERIEL ET METHODE
3.1. Matériel biologique ...................................................................................................... 12
3.2. Méthode ......................................................................................... 12
.................................................................................................... 12
3.3.1. Analyse physico-chimiques .................................................................................... 12
3.3.1.1. Détermination du pH ........................................................................................ 13
A) Principe ................................................................................................................. 13
B) Mode opératoire .................................................................................................... 13
3.3.1.2. Conductivité ..................................................................................................... 13
Sommaire
3.3.1.3. Détermination de la teneur en humidité ........................................................... 14
A) Principe ................................................................................................................. 14
B) Mode opératoire .................................................................................................... 14
C) Expression des résultats ........................................................................................ 15
.................................................................... 15A) Principe ................................................................................................................. 15
B) Mode opératoire .................................................................................................... 15
C) Expression des résultats ........................................................................................ 16
3.3.1.5. Détermination de la teneur en cendres ............................................................. 16
A) Principe ................................................................................................................. 16
B) Mode opératoire .................................................................................................... 17
C) Expression des résultats ........................................................................................ 17
3.3.1.6. Dosage des éléments minéraux ........................................................................ 18
Mode opératoire ......................................................................................................... 18
A. Pour Calcium Ca+2 .................................................................................................... 19
Principe du dosage .......................................................................................... 19
Mode opératoire ..................................................................................................... 19
B. Pour Magnésium Mg2+ .......................................................................................... 20
3.3.1.7. Dosage des sucres ............................................................................................. 20
3.3.1.8. Préparation sirop de la datte ............................................................................. 20
A) Mode opératoire ................................................................................................... 20
3.3.1.9. Dosage des sucres réducteurs ........................................................................... 21
A) Principe ................................................................................................................. 21
3.3.1.10. Préparation des échantillons pour la défécation ............................................. 21
Le principe .......................................................................................................... 21
Préparation du filtrat ........................................................................................... 22
A. Réduction de la solution cuivrique (Cu2+ ........................... 22 ................................................................. 23 C. Oxydation du précipité de Cu2O par une solution ferrique (Fe3+) ...................... 23D. Dosage du fer ferreux formé (Fe2+) par manganimétrie ...................................... 24
Expression des résultats ..................................................................................... 24
3.3.1.11. Dosage des sucres totaux................................................................................ 25
A. Expression de résultats ......................................................................................... 25
3.3.1.12. Teneur en saccharose ..................................................................................... 25
3.3.1.13. Taux de Fibre ................................................................................................. 25
Sommaire
A) Mode opératoire ................................................................................................... 25
B) Expression de résultats ......................................................................................... 25
3.3.1.14. Indice de qualité ............................................................................................. 25
Chapitr 4. RESULTATS ET DISCUSSIONS
4.1. Teneur en humidité ..................................................................................................... 28
4.2. Taux de la matière sèche ............................................................................................. 28
4.3. pH .................................................................................................................................. 29
4.4. Conductivité électrique ............................................................................................... 30
4.5. Acidité titrable ............................................................................................................. 31
4.6. Teneur en cendres ........................................................................................................ 32
4.7. Les fibres ...................................................................................................................... 33
4.8. Les Eléments minéraux ............................................................................................... 34
4.8.1. Les macroéléments .................................................................................................. 34
4.8.1.1. Sodium (Na+) .................................................................................................... 34
4.8.1.2. Le Potassium (K+) ........................................................................................... 35
4.8.1.3. Calcium (Ca2+) ................................................................................................. 36
4.8.1.4. Magnésium (Mg2+) ........................................................................................... 37
4.8.2. Oligoéléments ......................................................................................................... 38
4.8.2.1. Le Zinc (Zn2+) ................................................................................................. 38
4.8.2.2. Cuivre (Cu2+) .................................................................................................... 39
4.8.2.3. Le fer (Fe) ......................................................................................................... 40
4.9. Taux de sucres .............................................................................................................. 41
4.9.1. Sucres totaux ........................................................................................................... 41
4.10. Indice de qualité ......................................................................................................... 44
4.10.1. Evaluation de la qualité de datte ........................................................................... 45
4.10.1.1. Humidité ......................................................................................................... 45
4.10.1.2. pH ................................................................................................................... 46
4.10.1.3. Sucre totaux .................................................................................................... 46
Conclusion ............................................................................................................................... 49
Référence Bibliographique .................................................................................................... 51
Annexes
Résumé
Liste des tableaux
IListe des tableaux
Tableau 1. Production de la datte en 2016 (Faostat, 2017). ..................................................... 2
Tableau 2.
et al.,1983). ............................................................................................................................... 10
Tableau 3. Teneur en eau (Humidité) des dix variétés des dattes. .......................................... 28
Tableau 4. Taux de matière sèche des dix variété des dattes. ................................................. 29
Tableau. pH de la pulpe des dix variété des dattes. .............................................................. 29
Tableau 6. Teneur en conductivité électrique de la pulpe des dattes. ..................................... 30
Tableau . Acidité titrable de la pulpe des dattes.................................................................... 31
Tableau 8. Teneur en cendre des dix variété des dattes. ........................................................ 32
Tableau 9. Taux des fibres des variété des dattes. .................................................................. 34
Tableau 14. Teneur de potassium (mg pour 100 g de sirop brut) des dix variétés des dattes. 35 Tableau 15. Teneur de Calcium (mg pour 100 g de sirop brut) des dix variétés des dattes. .. 36 Tableau 16. Teneur de Magnésium (mg pour 100 g de sirop brut) des dix variétés des dattes................................................................................................................................................... 37
Tableau 10. Teneur de Zinc (mg pour 100 g de sirop brut) des dix variétés des dattes. ......... 38
Tableau 11. Teneur de cuivre (mg pour 100 g de sirop brut) des dix variétés des dattes. ...... 39
Tableau 12. Teneur de fer (mg pour 100 g de sirop brut) des dix variétés des dattes. ........... 40
Tableau 17. Teneur de sucres totaux des variétés des dattes. ................................................ 41
Tableau 18. Teneur de sucres réducteurs des variétés des dattes. .......................................... 42
Tableau 19. Teneur en saccharose des variétés des dattes. ..................................................... 43
Tableau 20. Indice de qualité des variétés des six variété des dattes. ..................................... 44
Liste des figures
IIListe des figures
Figure 1. Schéma du palmier dattier (Munier, 1973). ............................................................... 4
Figure 2. schéma datte et son noyau (Belguedj, 2001). ............................................................ 6
Figure 3. Composition biochimique globale de la datte (Sawayaet al., 1983). ......................... 8
Figure 4. Photo des différentes dattes étudies : A: Litima ; B-Mech Degla ; C-Degla Beida ; D-Deglet Nour ; E-Ghars ; F-Thouri ; G-Tantbouchet ; H-Horra ; I-Heloua ; K-Archti. ........ 12Figure 5 : Mesure du pH de l'échantillon à l'aide d'un pH-mètre. ........................................... 13
Figure 6. Echantillon après étuvage. ....................................................................................... 14
Figure 7. Titrage volumique de l'extrait de la datte. ................................................................ 16
Figure 8. Les capsules au four à moufle .................................................................................. 17
Figure 9. les extraits des sels minéraux pour leur dosage. ...................................................... 18
Figure. Photomètre à flamme. ............................................................................................ 19
Figure. Spectrophotomètre d'absorption atomique. ............................................................ 19
Figure 12 : titrage par EDTA. ................................................................................................. 20
Figure 13. sirop des dattes. ...................................................................................................... 21
Figure 14. L'échantillon après défécation................................................................................ 22
Figure 15. Réduction de la solution cuivrique. ....................................................................... 23
Figure 16. Oxydation du précipité de Cu2O par une solution ferrique ................................... 24
Figure 17 : Titrage volumique de sucres réducteurs. .............................................................. 24
Figure 18. Teneur en eau des variétés des dattes. ................................................................... 28
Figure 19. Matière sèche des variété des dattes. ..................................................................... 29
Figure 20. pH Des varietés des dattes .................................................................................... 30
Figure 21. Teneur en conductivité électrique des variétés des dattes. .................................... 31
Figure 22. Acidité titrable de la pulpe des dattes. ................................................................... 32
Figure 23. Teneur en cendre de variétés des dattes. ................................................................ 33
Figure 24. Les fibres des variété des dattes. ............................................................................ 34
Figure 25. La Teneur de sodium (mg pour 100 g de sirop brut) des variétés des dattes. ....... 35
Figure 26. La Teneur de potassium (mg pour 100 g de sirop brut) des variétés des dattes. ... 36
Figure 27. La Teneur de Ca2+ (mg pour 100 g de sirop brut) des variétés des dattes. ........... 37
Figure 28. La Teneur de Magnésium (mg pour 100 g de sirop brut) des dix variétés desdattes. ........................................................................................................................................ 38
Figure. La Teneur de zinc (mg pour 100 g de sirop brut) des variétés des dattes. ............. 39
Figure 30. La Teneur de cuivre (mg pour 100 g de sirop brut) des dix variétés des dattes. ... 40
Liste des figures
IIIFigure 31. La Teneur de Fer (mg pour 100 g de sirop brut) des variétés des dattes. .............. 41
Figure 32. La Teneur de sucres totaux des variétés des dattes. .............................................. 42
Figure 33. La Teneur de sucres totaux des variétés des dattes. .............................................. 43
Figure 34. La Teneur en saccharose des variétés des dattes. .................................................. 44
Figure 35. Indice de qualité des variétés des six variété des dattes. ........................................ 45
Figure 36.
Figure 37. .............................. 46
Figure 38 . ariétés par rapport aux
teneurs en sucres totaux ............................................................................................................ 46
Liste des abréviations
IVListe des abréviations
A %: Acidité titrable
Cd: La teneur en cendres
Ca2+ : Calcium
Cu : Cuivre
EDTA: Acide aminopolycarboxylique
H%: Humidité en pourcent
HCL : acide chlorhydrique
I.P.G.R.I : Institut International des Ressources PhytogénétiquesK+ : Potassium
Mo : Matière organique
Mg2+ : Magnésium
Na2+ : Sodium
NAOH : hydroxyde de sodium pH : Potentiel HydrogèneT (net) : Noir d'eriochrome T.
µs : Microsiemens
Zn2+ : Zinc
r : Indice de qualitéCB(%) : Taux de fibre
MS : Matière sèche.
H2SO4: Acide sulfurique.
DSA : Direction des Services Agricoles
Introduction
Introduction
Introduction générale
Le palmier dattier (Phoenix dactylifera L.) est la plus important culture des zones arides et semi-arides. Elle joue un rôle important dans la vie économique et sociale des populations de ces régions (Besbes et al., 2003) Avec une production mondiale de 8460443 tones et en algerie plus de 11 million de tones sur une superficies de 167269 hectares. inventoriés (Hannachi et al. 1998). En terme de production, biskra est la première wilaya phonicicole en Algérie, elle produit plus 41% des datte algériennes et ses palmeraies couvrentplus de 85% de la superficie totale dédiés à l'arboriculture fruitière dans la wilaya (DSA Biskra,
2016) . Des travaux ont été réalisés déjà sur les palmier dattier en Algérie comme ceux effectués
par Belguedj (2002) et Hannachi, Benkhalifa, Khitri et al., (1998), Egalement Bousdira (2007) En plus des travaux réalisés aux Ziban comme ceux de Djennane et Atia (2012), Djoudi (2013) dattier moyennent la caractérisation biochimique. En plus de sa consommation directe, la datte peut être utilisée caussi de fournir des informations sur leur utilisation en particulier dans des procèdes
biotechnologies (Oueld El Hadj etal.,2001).sauvegarder et de valoriser ce produit local afin de leur utilisation dans les différents domaines
économiques et industriels et leur pérennisation. Vu le peu et le manque des études et les analyses biochimiques sur les dattes, nous mené ce travail sur les analyses physico-chimiques des dattes.Le but de notre étude est la caractérisation physico chimique des quelques variétés de datte de
la région de Ziban. Le présent travail est divisé on deux grandes parties, une revue bibliographiquecomprenant deux chapitres dont le premier est généralité sur le palmier dattier, le deuxième le
fruit (datte).dattes de dix cultivars et leur évaluation, où nous avons tenu compte des caractères
Introduction
biochimiques. Aussi nous avons eser la qualité dattière de nos cultivars en faisant appel à des normes portant sur des caractères biochimique.Partie bibliographique
¾ Partie bibliographique
Chapitre 1 : Généralités sur le
Palmier dattier
Le palmier dattierChapitre 1
1.1.Généralités sur le palmier dattier
Le palmier dattier (Phoenix dactylifera L.), provient du mot "Phoenix» qui signifiedattier chez les phéniciens, et dactylifera dérive du terme grec "dactylos» signifiant doigt,
allusion faite à la forme du fruit (Djerbi, 1994). C'est une espèce dioïque, monocotylédone
arborescente, appartenant à une grande famille d'arbre à palmes produisant des dattes (Mazoyer,
2002).
Le dattier est une monocotylédone probablement originaire du golfe persique (Gilles,2000). Le palmier dattier est cultivé comme arbre fruitier dans les régions chaudes arides et
semi-arides. Le dattier est une espèce thermophile ; il exige un climat chaud, sec et ensoleillé.
al. 1990), grâce à sa remarquable adaptation aux conditions climatiques, la haute valeur nutritive de ses fruits, les multiples utilisations de ses produits (Bousdira et al. 2003 ; Bakkaye, 2006). Tableau 1. Production de la datte en 2016 (Faostat, 2017).Monde Algérie superficies Ha 1353159 167269 rendement Kg/Ha 62524 61550 production en Tone 8460443 1029596
1.2. Position systématique
Le genre Phoenix appartient à la famille des Arecaceae (anciennement, Palmacée) comprend environ 2500 espèces (Dransfied et al., 2008). Le genre Phoenix comporte au moins (Espirad, 2002). La classification botanique du palmier dattier donnée par (Djerbi, 1994) est la suivante:Groupe : Spadiciflores
Embranchement : Angiospermes
Classe : Monocotylédones
Ordre : Palmales
Le palmier dattierChapitre 1
Famille : Palmacées
Sous famille : Coryphoidées
Genre : Phoenix
Espèce : Phoenix dactylifera L.1.3. Biologie du palmier dattier
La multiplication du palmier dattier se fait donc par1.3.1. La reproduction sexuée
La multiplication par semis de graine est la méthode traditionnelle la plus anciennement pratiquée par les phoeniciculteurs. Elle a permis la création de nombreuse palmeraies et l'extension des cultures en dehors de son aire d'origine (Munier, 1973).1.3.2. La reproduction asexuée
1.3.2.1. Rejet : reproduit intégralement les caractéristiques du pied mère.
méthode la utilisée par les phoeniciculteurs pour la reproduction du dattier.1.3.2.2. Gourmand ou roukab : les gourmands se développent haut sur le tronc ou sur
très forte tendance à dégénérer.1.3.2.3. Culture in vitro : face aux maladies cryptogamiques et pour pallier aux
problèmes de disparition des variétés ne présentant peu ou plus de rejets, (Chaibi et al., 2002).
1.4. Morphologie du palmier dattier
Ont décrit la description morphologique de palmier dattier comme suit :1.4.1. Organes végétatifs
1.4.1.1. Le système racinaire
Note que le système racinaire est de type fasciculé volumineux et est émergé en partie au-dessus du niveau du sol (Munier, 1973).1.4.1.2. Le stipe ou tronc
Décrit ne structure
très particulière.1.4.1.3. Les feuille
Les feuilles du dattier sont appelées palmes ou djerids, elles ont une forme pennée et sont insérées en hélice, très rapprochées sur le stipe (Belhabib, 1995).Le palmier dattierChapitre 1
1.4.1.4. Les organes floraux
D2000) tous les Phoenix, et donc le palmier dattier, sont des arbresdioïques. Les sexes étant séparés. Les fleurs sont portées par des pédicelles, ou des épillets qui
sont à leur tour sont portés par un axe charnu, la hampe ou spadice.1.4.1.5. La fleur femelle
corolle formée de 3 pétales ovales et arrondies. Le gynécée comprend 3 carpelles indépendants
à un seul ovule (Munier, 1973).
1.4.1.6. La fleur mâle
de 3 pétales légèrement allongées formant la corolle. La fleur possède 6 étamines à déhiscence
interne et trois pseudo-carpelles (Belhabib, 1995). Figure 1. Schéma du palmier dattier (Munier, 1973).Chapitre : 2
La datte
La datte 2 Chapitre
2.1. Description de la datte
La datte, fruit du palmier dattier, est une baie appelée " Datte, Tmar en arabe»,
consistance dure, entouré de chair. La partie comestible de la datte, dite chair ou pulpe, est constituée de : Un péricarpe ou enveloppe cellulosique fine dénommée peau. Un mésocarpe généralement charnu, de consistance variable selon sa teneur en sucre et est de couleur soutenue. Un endocarpe de teinte plus claire et de texture fibreuse, parfois réduit à une membrane parcheminée entourant le noyau (Espiard, 2002)à 8 grammes selon les variétés. Leur couleur va du blanc jaunâtre au noir en passant par les
couleurs ambre, rouges, brunes plus ou moins foncées (Djerbi, 1994). La figure 2 montre une coupe de la datte et de son noyau. Figure 2. schéma datte et son noyau (Belguedj, 2001).2.2. Classification des dattes
2.2.1. Selon la consistance des dattes
D'après (Espirad, 2002) Classification des dattes selon leur consistance est variable. Selon cette caractéristique, les dattes sont réparties en trois catégories :La datte 2 Chapitre
2.2.1.1 Les dattes molles :
de sucres invertis (fructose, glucose) telle que : Ghars, Litima.2.2.1.2 Les dattes demi- molles : de 20 à 30% : Deglet-Nour, Hamraia.
2.2.1.3 Les dattes sèches :
Elles Sont de texture farineuse telles que : Degla-Beida, Mech-Degla.2.2.2. Selon des qualités commerciales
2.2.2.1. Dattes fines ou exportables : dont le type est représenté par la Deglet Nour.
2.2.2.2. Dattes communes : représenté par Ghares ; Degla Beida
2.3. Formation et maturation de la datte
Les fleurs fécondées à la nouaison, donnent un fruit qui évolué en taille, en consistance
et en couleur ju(Gilles, 2000).Chaque étape de la maturation de la datte a été t au cours de son développement (Munier, 1973). Les différents stades peuvent être définis comme suit :2.3.1. Stade Hababouk : immédiatement la pollinisation. La datte
5 semaines après la pollinisation (Djerbi, 1994).
2.3.2. Stade Khalal : selon (1946, Rygg), La datte commence son développement, grossit
4-7 semaines. Le goût de la datte à ce stade est astringent à cause de la présenc
important de tanins (Beker, 2002).2.3.3. Stade Bser : Selon le descripteur du palmier dattier (IPIGRI)
développement de la datte durant lequel, le fruit prend sa forme et sa taille finale, et il passe de
sa couleur verte à une couleur généralement jaune ou rouge, rarement verdâtre. La période de
quotesdbs_dbs10.pdfusesText_16[PDF] diholoside réducteur et non réducteur
[PDF] pouvoir réducteur des glucides
[PDF] le système hormonal
[PDF] glandes endocrines et hormones
[PDF] système endocrinien pour les nuls
[PDF] liste des hormones pdf
[PDF] type d'hormone
[PDF] les hormones et leurs fonctions pdf
[PDF] lipides simples et complexes
[PDF] classification des microorganismes ppt
[PDF] le monde microbien wikipedia
[PDF] tableau de classification des micro-organisme
[PDF] pfe pont dalle
[PDF] pont a poutre en béton armé pdf
