 Chapitre 1 :Classification périodique des éléments
Chapitre 1 :Classification périodique des éléments
https://www.immae.eu/cours/. Page 2. Chapitre 1 : Classification périodique des éléments. Structure de la matière. Page 2 sur 5. 118? Th. 75.6 ?In. 95. Di. 60 ?
 Chapitre IV : Classification périodique des éléments
Chapitre IV : Classification périodique des éléments
15 avr. 2020 Le tableau périodique actuel classe les éléments par numéro atomique Z croissant. Il diffère peu de la classification selon l'ordre croissant ...
 Chapitre II: La classification périodique X
Chapitre II: La classification périodique X
Les éléments d'une même période ont le même nombre quantique principal n. Les éléments appartenant à une même colonne ont généralement la même structure.
 Chapitre 5 : La classification périodique des éléments
Chapitre 5 : La classification périodique des éléments
A RETENIR : - Dans le tableau périodique des éléments actuel les éléments chimiques sont classés par numéro atomique. (Z) croissant ;.
 Chapitre I - Classification périodique des éléments
Chapitre I - Classification périodique des éléments
Les éléments du syllabus sur lesquels portera le test du comité français des http://www.cayrel.net/?Cours-P1-Mecanique. Page 3. IPHO Lycée Jean Perrin. 3 ...
 Chimie générale
Chimie générale
Lieu du cours. Louvain-la-Neuve. Thèmes abordés. - Structure de l'atome. - Classification périodique des éléments. - Liaisons chimiques. - Structures de Lewis
 1 Classification périodique des éléments
1 Classification périodique des éléments
Présentation d'une case du tableau : Cette présentation est classique mais elle offre à ce stade du cours trop d'informations. En ce qui concerne l'étude du
 Chapitre 9 : La classification périodique des éléments
Chapitre 9 : La classification périodique des éléments
Cet outil est très important pour le chimiste car il lui permet de prévoir le comportement d'un élément chimique au cours d'une réaction. Le tableau périodique.
 Eléments de chimie inorganique et analytique
Eléments de chimie inorganique et analytique
Université catholique de Louvain - Eléments de chimie inorganique et analytique - cours-2022-lchm1231 position dans le tableau de classification périodique. L ...
 CHAPITRE V Classification Périodique des éléments
CHAPITRE V Classification Périodique des éléments
1)- Classification des éléments dans le tableau périodique: couche d incomplète soit à l'état fondamental soit au cours d'une réaction chimique.
 Chapitre 1 :Classification périodique des éléments
Chapitre 1 :Classification périodique des éléments
Conservation de la quantité de ces éléments au cours d'une réaction chimique quelconque. Dalton : La matière est constituée d'atomes. Les éléments chimiques
 Chapitre IV : Classification périodique des éléments
Chapitre IV : Classification périodique des éléments
Le tableau périodique actuel classe les éléments par numéro atomique Z croissant. Il diffère peu de la classification selon l'ordre croissant des masses
 La classification périodique des éléments
La classification périodique des éléments
Chapitre 3 : La classification périodique des éléments. Pierre-Alexis GAUCHARD. Agrégé de chimie Docteur ès sciences. UE1 : Chimie – Chimie physique.
 Lunivers Chapitre 6 : la classification périodique des éléments
Lunivers Chapitre 6 : la classification périodique des éléments
On classe actuellement les éléments chimiques dans un tableau. Le tableau périodique des éléments comporte 112 éléments chimiques connus.
 Chapitre 9 : La classification périodique des éléments
Chapitre 9 : La classification périodique des éléments
Cet outil est très important pour le chimiste car il lui permet de prévoir le comportement d'un élément chimique au cours d'une réaction.
 Chapitre 5 : La classification périodique des éléments
Chapitre 5 : La classification périodique des éléments
En 1869 Mendeleïev est le premier à avoir l'idée de classer les éléments chimiques par « poids » atomiques. (maintenant appelée masse atomique) croissant en s'
 Chapitre II: La classification périodique X
Chapitre II: La classification périodique X
Les éléments d'une même période ont le même nombre quantique principal n. Les éléments appartenant à une même colonne ont généralement la même structure.
 Classification périodique des éléments chimiques
Classification périodique des éléments chimiques
Et avec la croissance du nombre d'éléments chimiques découverts et artificiels au cours des 17ème et 18ème siècles leur ordre et leur organisation selon des
 Architecture de la matière
Architecture de la matière
Chapitre 4.1 : élément et atome. Chapitre 4.2 : la classification périodique des éléments. Chapitre 3 : molécules et solvants. Cours de chimie de première
 [PDF] Chapitre 5 : La classification périodique des éléments - AlloSchool
[PDF] Chapitre 5 : La classification périodique des éléments - AlloSchool
- Dans le tableau périodique des éléments actuel les éléments chimiques sont classés par numéro atomique (Z) croissant ; - Les éléments chimiques dont les
 [PDF] Chapitre 1 :Classification périodique des éléments - Melusine
[PDF] Chapitre 1 :Classification périodique des éléments - Melusine
Mendeleïev réalise une classification pour M croissant en faisant apparaître sur une même ligne des éléments qui ont les mêmes propriétés chimiques Chapitre 1
 [PDF] Chapitre IV : Classification périodique des éléments
[PDF] Chapitre IV : Classification périodique des éléments
15 avr 2020 · Le tableau périodique actuel classe les éléments par numéro atomique Z croissant Il diffère peu de la classification selon l'ordre croissant
 [PDF] Chapitre IV : Classification périodique des éléments
[PDF] Chapitre IV : Classification périodique des éléments
La classification périodique est basée sur la formation de groupes constitués par les éléments possédant des propriétés chimiques analogues On regroupe dans
 [PDF] CHAPITRE V Classification Périodique des éléments
[PDF] CHAPITRE V Classification Périodique des éléments
Chapitre V: Classification Périodique des éléments 69 Sous- couche S p d f 3)- Le nombre quantique magnétique m : Il définit les orientations dans
 [PDF] Chapitre II: La classification périodique (Tableau périodique)
[PDF] Chapitre II: La classification périodique (Tableau périodique)
Les éléments d'une même période ont le même nombre quantique principal n Les éléments appartenant à une même colonne ont généralement la même structure
 [PDF] Tableau périodique des éléments chimiques (2016)
[PDF] Tableau périodique des éléments chimiques (2016)
Tableau périodique des éléments Numéro atomique Principaux nombres d'oxydation (le plus fréquent en gras) Configuration électronique (en rouge
 [PDF] la classification périodique des éléments - Chimie en PCSI
[PDF] la classification périodique des éléments - Chimie en PCSI
Chapitre 3 : molécules et solvants Cours de chimie de première période de PCSI I HISTORIQUE DE LA CLASSIFICATION PERIODIQUE DES ELEMENTS CHIMIQUES
Comment sont classés les éléments dans la classification périodique ?
Dans la classification périodique, les éléments sont classés par numéro atomique Z croissant. La classification périodique des éléments comporte 7 lignes et 18 colonnes. Les lignes ou périodes représentent le nombre de couches électroniques autour du noyau de l'atome correspondant.Quelles sont les 3 règles de construction du tableau périodique actuelle ?
Il dicte alors les points clés de sa théorie : Les propriétés des éléments sont périodiques quand ils sont rangés selon leur masse atomique. Les éléments possédant des propriétés semblables ont des masses atomiques proches. L'arrangement des éléments correspond à peu près à leurs valences.Comment déterminer la position d'un élément dans le tableau périodique PDF ?
Le numéro de la dernière couche qui contient des électrons indique le numéro de la ligne, appelée période, dans laquelle se trouve d'atome. Le nombre d'électrons de la dernière couche indique le numéro de la colonne du tableau simplifié, auquel on ajoute 10 pour avoir le numéro de la colonne dans le tableau complet.- La première colonne est nommée famille des alcalins, la deuxième colonne est nommée famille des alcalino-terreux, l'avant-dernière colonne est nommée famille des halogènes et, enfin, la dernière colonne est nommée famille des gaz inertes (ou gaz rares).
Classe de 2nd Chapitre 9
Chimie
1 Chapitre 9 : La classification périodique des élémentsIntroduction :
Cet outil est très important pour le chimiste car il lui permet de prévoir le comportement d"un élément chimique au cours d"une réaction. Le tableau périodique rassemble également les principales informations sur un élément chimique dont un chimiste peut avoir besoin. Nous verrons ici comment a été établit le tableau historiquement parlant mais aussi comment on l"utilise de nos jours.I Le tableau périodique : (voir TP n°9)
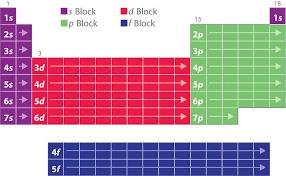
1) Sa construction :
C"est le tableau de Mendeleïev de 1869 qui a servit de base à la construction de la classification actuelle. Les principales caractéristiques sont les suivantes : Les éléments sont rangés par numéro atomique croissant.Le tableau compte des lignes et des colonnes :
A chaque ligne appelée période, on remplit une couche électronique différente (Pour la 1 ère on remplit la couche K, pour la seconde on remplit la couche L, pour la troisième on remplit la couche M). Les éléments dont les atomes ont le même nombre d"électrons sur leur couche externe ou périphérique sont disposés dans une même colonne.2) Notion de famille :
Les éléments d"une même colonne forment une famille. Ils ont des propriétés chimiques voisines.3) Notion de périodicité :
Le tableau est nommé tableau périodique (qui revient régulièrement) car on retrouve les éléments avec même propriétés à des intervalles réguliers (donc en colonne).II Les familles d"éléments :
1) Familles des Alcalins :
Elle rassemble les éléments de la première colonne mis à part l"hydrogène. Ils ont un électron sur leur couche externe qu"ils perdent facilement pour donner des ions de charger +e : Li +, Na+ et K+. Ce sont des métaux mous qui réagissent très vivement avec l"eau.2) Famille des halogènes :
Ce sont les éléments de la XVII
ème colonne.
Ils ont 7 électrons sur leur couche externe et vont donc facilement en gagner un pour former des ions de charge -e : F -, Cl-, Br-, I-. Dans la nature, ils se trouvent sous cette forme d"ion ou sous forme de molécules diatomiques (fortement toxiques).Classe de 2nd Chapitre 9
Chimie
23) Famille des gaz rares ou nobles :
Elle contient les éléments de la XVIII
ème colonne : He, Ne, Ar, Kr, Xe.
Ce sont les éléments chimiques les plus stables, ils sont inertes chimiquement. Ils sont doncgazeux et très peu présents dans l"atmosphère terrestre mis )à part l"hélium, deuxième
élément le plus abondant dans l"univers après l"hydrogène. III Quelles informations nous apportent la classification :1) Charges des ions monoatomiques :
Tous les éléments d"une même famille vont formés des ions de même charge afin d"obéir à la
règle de l"octet.Famille
Alcalins Famille du
Béryllium Famille du
Bore Famille de
l"azote Famille de l"Oxygène Halogène Ions formés Li+ ; Na+ ; K + Be 2+ ; Mg 2+ ; Ca 2+ B3+ ; Al3+ N3- ; P3- O2- ; S2- F
- ; Cl- ; Br - ; I-Charge
des ions +e +2e +3e -3e -2e eOn rappelle que les éléments gagnent ou perdent des électrons pour acquérir la configuration
électronique (stable) du gaz rare le plus proche dans la classification.2) Nombre de liaisons covalentes qu"un élément peut former :
Le nombre de liaisons covalentes qu"un atome doit former est égal au nombre d"électrons qu"il doit gagner pour obéir à la règle de l"octet.Famille
Nombre de
liaisons formées :Carbone 4
Azote 3
Oxygène 2
Halogène 1 Exercices n°10, 11, 12, 15, 17 p121-122quotesdbs_dbs9.pdfusesText_15[PDF] classification phylogénétique des animaux cycle 3
[PDF] classification phylogénétique simplifiée
[PDF] classification phylogénétique definition
[PDF] classification phylogénétique des végétaux
[PDF] arbre phylogénétique des embryophytes
[PDF] chlorobionte
[PDF] classification embryophytes
[PDF] lignée brune
[PDF] lignée verte classification
[PDF] rhodobionte
[PDF] endosymbiose primaire définition
[PDF] embryophytes définition
[PDF] classification phylogénétique du vivant 4ème édition
[PDF] pourquoi enseigner la classification du vivant
