 dosage manganimetrie
dosage manganimetrie
- : ion permanganate oxydant puissant
 les dosages oxydo-reductimetriques (redox) - la manganimetrie
les dosages oxydo-reductimetriques (redox) - la manganimetrie
La manganimétrie permet le dosage d'un grand nombre de réducteurs car MnO4. - 1-1) Potentiel d'oxydo-réduction : *La méthode iodométrique est basée sur la ...
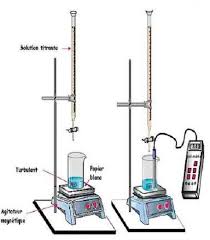 Les Travaux Pratiques De Réactivité chimique
Les Travaux Pratiques De Réactivité chimique
molaire. La concentration massique. NB ± ∆NB. CB ± ∆CB. C'B ± ∆C'B. Page 27. Page - 26 -. TP N° 2. DOSAGE D'OXYDOREDUCTION : Manganimétrie. Quel est le but
 TP Nº5 (Semestre 2) : Dosage doxydo-réduction
TP Nº5 (Semestre 2) : Dosage doxydo-réduction
La manganimétrie consiste à doser des solutions réductrices de normalité inconnue au moyen de l'agent oxydant (MnO4) en milieu acide. Page 2. 2. Dosage d'oxydo-
 TRAVAUX PRATIQUES DE CHIMIE I
TRAVAUX PRATIQUES DE CHIMIE I
Dosage Oxydoréduction (manganimétrie). Page 30. Dosage Oxydoréduction (manganimétrie). I. Objectif. ✍ Il s'agit de déterminer le titre molaire d'une solution
 TP Nº5 (Semestre 2) : Dosage doxydo-réduction
TP Nº5 (Semestre 2) : Dosage doxydo-réduction
La manganimétrie consiste à doser des solutions réductrices de normalité inconnue au moyen de l'agent oxydant (MnO4) en milieu acide. Page 2. 2. Dosage d'oxydo-
 Dosage du fer ferreux La manganimétrie est une technique
Dosage du fer ferreux La manganimétrie est une technique
TP n°3 OXYDOREDUCTION : MANGANIMETRIE. APPLICATION : Dosage du fer ferreux. La Pour l'étalonner on utilisera un réducteur. Utiliser une solution ...
 Manipulation N° III: Dosage par la méthode doxydo-réduction
Manipulation N° III: Dosage par la méthode doxydo-réduction
Manganimétrie : C'est une méthode basée sur les réactions d'oxydation par l'ion permanganate. L'oxydation peut être effectuée en milieu acide alcalin ou en
 Travaux Pratiques de Chimie Générale Manganimétrie
Travaux Pratiques de Chimie Générale Manganimétrie
• On appelle manganimétrie l'ensemble des dosages d'oxydo-réduction utilisant comme solution oxydante le permanganate de potassium KMnO4. • Les propriétés
 Chimie analytique 2éme année pharmacie -Les réactions d
Chimie analytique 2éme année pharmacie -Les réactions d
Définition d'une réaction d'oxydo-réduction : Une réaction d'oxydoréduction (dosage en retour) => manganimétrie. • Milieu alcalin : −/ −. Exemple : ...
 dosage manganimetrie
dosage manganimetrie
- : ion permanganate oxydant puissant
 Les Travaux Pratiques De Réactivité chimique
Les Travaux Pratiques De Réactivité chimique
DOSAGE D'OXYDOREDUCTION : Manganimétrie. Généralités. Rappels. Selon les conceptions de la chimie électronique le processus d'oxydation ou de réduction se
 Dosage du fer ferreux La manganimétrie est une technique
Dosage du fer ferreux La manganimétrie est une technique
TP n°3 OXYDOREDUCTION : MANGANIMETRIE Pour l'étalonner on utilisera un réducteur. ... 2- Application : Dosage du fer ferreux
 Chimie analytique 2éme année pharmacie -Les réactions d
Chimie analytique 2éme année pharmacie -Les réactions d
METHODES D'ANALYSE TITRIMITRIQUE EN OXYDOREDUCTION. Manganimétrie : I- Introduction : Les dosages manganimétrique mettent en jeu le pouvoir oxydant de l'ion
 TRAVAUX PRATIQUES DE CHIMIE I
TRAVAUX PRATIQUES DE CHIMIE I
Dosage Oxydoréduction (manganimétrie). I. Objectif. ? Il s'agit de déterminer le titre molaire d'une solution de sulfate ferreux et par.
 TP CHIMIE-1 & TP CHIMIE-2
TP CHIMIE-1 & TP CHIMIE-2
TP IV : Dosage (Titrage) d'oxydo-réduction . à l'aide d'indicateurs colorés d'oxydoréduction. Le dosage ... sont à l'origine de la manganimétrie.
 Manipulation N°4 Dosage doxydo-réduction : 1- Introduction : 2- But
Manipulation N°4 Dosage doxydo-réduction : 1- Introduction : 2- But
Dosage (Titrage) d'oxydo-réduction Le dosage consiste à déterminer la normalité d'une solution réductrice ... Ce dosage est appelé manganimétrie.
 TP N° 02. DOSAGE DES IONS FER (Fe ) CONTENUS DANS LE
TP N° 02. DOSAGE DES IONS FER (Fe ) CONTENUS DANS LE
DOSAGE DES IONS FER (Fe. 2+. ) CONTENUS DANS LE SEL DE MOHR. PAR MANGANIMETRIE. 1. INTRODUCTION. Les réactions d'oxydoréduction ou réactions redox
 GÉNÉRALISATIO DE LOXYDO-RÉDUCTION EN SOLUTION
GÉNÉRALISATIO DE LOXYDO-RÉDUCTION EN SOLUTION
Peut-on doser une solution de chlorure de fer (II) par manganimétrie ? 23. Quelle est l'équation-bilan de la réaction de l'acide nitrique sur les ions fer (II).
 Les dosages doxydoréduction
Les dosages doxydoréduction
Les dosages d'oxydoréduction. Exercice 1 : Teneur en dioxyde de soufre dans un vin blanc. La teneur maximale en dioxyde de soufre d'un vin est imposée par
Isabelle Prigent
Chimie et développement durable EXERCICES Partie 1/ Chimie minérale
Exercice 1 : Teneur en dioxyde de soufre dans un vin blanc" La concentration massique en dioxyde de soufre ne doit pas dépasser 210 mg.L-1 dans un vin blanc »
Pour cela, il introduit dans un erlenmeyer, un volume V1 = (20,000,05) mL de vin blanc limpide très
La solution titrante, de concentration en diiode C2 = (1,000,01)×10ʹ2 mol.L-1 est ensuite ajoutée
0,05) mL de solution de diiode.
SO42-/SO2
ions iodure Iʹ, les ions sulfate SO42ʹ et le dioxyde de soufre en solution sont incolores.3) Déterminer la concentration molaire C1 en dioxyde de soufre de ce vin et en déduire sa concentration
massique Cm en dioxyde de soufre ; M(SO2) = 64,1 g.mol-14) Exprimer les valeurs de C1 et de Cm avec leurs incertitudes sachant :
2 2 2 2
1 2 2 1
1 2 2 1
UC UV (eq) UC UV
C V (eq) C
quotesdbs_dbs50.pdfusesText_50[PDF] dosage oxydoreduction pdf
[PDF] dosage par titrage colorimétrique
[PDF] dosage par titrage conductimétrique
[PDF] dosage par titrage conductimétrique destop correction
[PDF] dosage par titrage protocole
[PDF] dosage permanganate de potassium par acide oxalique
[PDF] dosage permanganate de potassium par sel de mohr
[PDF] dosage ph métrique definition
[PDF] dosage ph métrique tp
[PDF] dosage potentiométrique d'une solution de sel de mohr
[PDF] dosage potentiometrique equivalence
[PDF] dosage sulfate ferreux par permanganate de potassium
[PDF] dose mais par hectare
[PDF] dose toxique aspirine
