 Exercices : écritures de configurations électroniques
Exercices : écritures de configurations électroniques
Exercice 4 : configuration électronique de quelques ions. 1) Préciser la configuration électronique fondamentale des ions suivants : a) ion Cl- numéro
 Corrigé Examen de CHIMIE1 (GB113)
Corrigé Examen de CHIMIE1 (GB113)
Exercice 3 (95 pts : 38 x 0
 Type de Licence
Type de Licence
les éléments dont la configuration électronique de la couche de valence est semblable (à n prés) 5.7 Exercices corrigés. Exercice 01 : Écrivez les structures ...
 Rappels de cours & Exercices corrigés
Rappels de cours & Exercices corrigés
25 févr. 2023 Le cinquième chapitre traite la configuration électronique et la classification périodique des éléments chimiques. Le sixième chapitre est ...
 EXERCICES RATTRAPAGE SECONDE EXERCICES
EXERCICES RATTRAPAGE SECONDE EXERCICES
Donner sa configuration électronique. 2. Celle-ci respecte-t-elle la règle de l'octet ? Ex 7 – L'ion sodium. L'atome de
 Corrigé
Corrigé
Sous le titane Zr aura la configuration électronique
 Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points
Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points
3 mars 2020 Il va perdre 3 électrons pour obtenir 8 électrons sur la couche 2. Sa configuration électronique sera 1s22s22p6 . Il va donc former l'ion Al3+.
 01 - Tableau périodique et cfg élec
01 - Tableau périodique et cfg élec
Corrigé exercice 1. TABLEAU PÉRIODIQUE ET CONFIGURATIONS ÉLECTRONIQUES. 1). La Calcium et strontium ont leur configuration électronique se terminant par Q ...
 exercices corriges de structure de la matiere et de liaisons chimiques
exercices corriges de structure de la matiere et de liaisons chimiques
Donner sa configuration électronique et son numéro atomique. Exercice IV. 2. Trouver la configuration électronique des éléments suivants et donner les ions
 Travaux Dirigés de Licence – HLCH 101 - Chimie Générale – 2020
Travaux Dirigés de Licence – HLCH 101 - Chimie Générale – 2020
Ces exercices sont des extraits d'examen dont vous pourrez trouver pour certains des corrigés 2- Déterminer la configuration électronique fondamentale de Ti ...
 Exercices : écritures de configurations électroniques
Exercices : écritures de configurations électroniques
Exercice 4 : configuration électronique de quelques ions. 1) Préciser la configuration électronique fondamentale des ions suivants :.
 Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points
Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points
3 mars 2020 Exercice 1 : (4 points) configuration (ou structure) électronique d'un atome. Remplir le tableau suivant. Atomes. Nombre d'électrons.
 Cours de chimie Générale
Cours de chimie Générale
Chapitre I : Configuration électronique de l'atome. I.1. Nombres quantiques et orbitales atomiques. On peut expliquer la quantification de l'énergie avec le
 Cours de Chimie Structure de la matière
Cours de Chimie Structure de la matière
chapitres avec des exercices corrigés dans chaque chapitre. Exercice 01. 1) Etablissez la configuration électronique des éléments suivants :.
 Corrigé
Corrigé
EXERCICE 1 : NANOPARTICULES ET OXYDE DE. TITANE / 28 POINTS atomiques pour obtenir la configuration électronique d'un atome. En déduire la.
 X A Rb Rb
X A Rb Rb
Exercices Corrigés. Corrigé de Série n°1 : Exercices d'atomistique Exercice VIII. A) a- Etablir la configuration électronique des espèces chimiques F.
 Les familles des éléments chimiques (7 points) Deuxième exercice
Les familles des éléments chimiques (7 points) Deuxième exercice
Écrire la configuration électronique de cet atome. Corrigé. Barème. Premier exercice : Les familles des éléments chimiques (7 pts). 1. Le magnésium.
 Les familles des éléments chimiques (7 points) Deuxième exercice
Les familles des éléments chimiques (7 points) Deuxième exercice
Écrire la configuration électronique de cet atome. Corrigé. Barème. Premier exercice : Les familles des éléments chimiques (7 pts). 1. Le magnésium.
 jeudi 15 janvier 2015 CHIMIE PCSI CORRIGE Devoir Surveillé n°3
jeudi 15 janvier 2015 CHIMIE PCSI CORRIGE Devoir Surveillé n°3
15 janv. 2015 CHIMIE PCSI CORRIGE ... Exercice 1 : QCM et petites questions 20 min ... 1) Ecrire la configuration électronique fondamentale de l'atome de ...
 CORRIGE
CORRIGE
11 déc. 2015 CORRIGE. Exercice 1 : 22 points. Exercice 2 : 16 points ... 2) Donner la configuration électronique de l'atome de silicium.
 Exercices Chapitre 2 : Configuration électronique - Sadk
Exercices Chapitre 2 : Configuration électronique - Sadk
1 La configuration électronique du fluor est (b) 1s22s22p5 car la période indique le numéro de la couche externe et 7 le nombre d’électrons de valence 2 Le fluor fait partie de du bloc 2p car c’est le nom de la dernière sous-couche remplie Exercice 4:Reconnaître les éléments d’une même famille (a)1s1 (b)1s2 (c)1s22s22p5 (d
 Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points)
Devoir surveillé n°6 3/3/2020 seconde Exercice 1 : (4 points)
Exercice 1 : (4 points) configuration (ou structure) électronique d’un atome Remplir le tableau suivant Atomes Nombre d’électrons Configuration électronique Nombre d’électrons de valence Silicium(Si) Z = 14
 EXERCICES RATTRAPAGE SECONDE
EXERCICES RATTRAPAGE SECONDE
EXERCICES EXERCICES RATTRAPAGE SECONDE Ex 1 – Ecrire des configurations électroniques 1 L’atome de sodium possède 11 électrons Ecrire sa configuration électronique 2 L’atome d’hélium a pour notation symbolique 24???????? Ecrire sa configuration électronique 3 L’atome d’Argon appartient à la 18ème colonne de la 3ème
 Images
Images
1- Donner la composition de cet atome 2- Ecrire sa configuration électronque 3- L’ion fluorure est obtenu à partir de l’atome de fluor lorsque celui-ci gagne un électron 2crire la configuration électronique de l’ion fluorure Exercice 5 Le chlorure de sodium est composé des ions
DEVOIRCOMMUNN°2PHYSIQUE-CHIMIE______vendredi11décembre2 5______SUJETDECHIMIEDurée de la partie chimie : 2 heures L'usage de la calculatrice est autorisé ______ CORRIGE Exercice 1 : 22 points Exercice 2 : 16 points Barème sur 38 points - Noté sur 30 Moyenne : 7,91
Problème1:utilisationsdusilicium22ptIAtomistique-liaisonchimique1) Lesiliciumexisteàl'étatnaturelsouslestroisformessuivantes:1428Si:92,2%1429Si:4,7%1430Si:3,1%Estimerlamassemolaireatomiquedel'élémentSi.1ptPourcetteestimation,utilisonslespourcentagesdechaqueisotope:Lamassemola iredel'élémen ts'obtient enadditionnantlesmassesmolairesdesisotopesmultipliéesparleurabondanceatomique:M(Si)=0,922x28+0,047x29+0,031x30=28,109=28,11g.mol-1Lesmassesmolairessontpresqu'égalesaunombredemasseA.1molestlaquantitédematièreprésentedans12gdecarbone-12.Enprenantlamasseduprotonetduneutronégale,lamassede1neutron(oud'unproton)estdoncégaleà(12/12.N).AinsidansunatomeoùilyaNneutronsetZprotons,soitunnombredenucléonségalàA,nombredemasse,alorslamassemolairedecetatomeest:M=A.(12/12.N).N=Ag.mol-1Ainsi,M(élément)=sommedes(massesmolairesdesisotopesxabondanceatomique)Soit:"M(ZX)=S(M(AZX)x%(AZX))»2) Donnerlaconfigurationélectroniquedel'atomedesilicium.Quelleestlavalencedusilicium?0,5ptSaconfigurationélectroniquefondamentaleest:1s22s22p63s23p20,5ptSavalenceestlenombredeliaisonssimplesqu'ilpeutformerpourréaliserunoctetenrestantneutre.Illuifautquatreélectronspourcomplétersonoctet,quevontluiapporter quatreatomesd'hyd rogèneparexemple. Ainsi,commele carbone,lesiliciumesttétravalent.3) Danslacolonnedequelélément(basedelachimieorganique)setrouvelesilicium?D'aprèsleu rpositionrelativedanslaclass ificationpériodique,comparerqualitativementleurrayonatomiqueetleurélectronégativité.0,5ptSaconfigurationélectroniqueexterneestlamêmequecelledel'atomedecarboneCsituéejusteau-dessusdeluidanslaclassificationpériodique.Plusdedoutelorsquel'onditquec'estl'élémentdebasedetoutelachimieorganique.0,5ptCommeladimensionatomiqueaugmentequandondescenddansunecolonne,alorsl'atomedesiliciumestplusgrosquel'atomedecarbone.0,5ptCommel'électronég ativitéaugmentequandonmontedansunecolon ne,alorsl'atomedesiliciumestplusmoinsquel'atomedecarbone.SiplusgrosetmoinsélectronégatifqueC.
IIEtudestructuraledusilicium4) Lesiliciumcristallisedanslemêmesystèmecristallinquelecarbonediamant:lamailleconventionnelleestunemailled'unestructurecubiqueàfacescentréesd'atomesdesiliciumdontunsite tétraédrique surdeuxest occupépa runatomedesilicium.Dessinerlamailleélémentairedelastructuredusilicium.1ptMaillesemblableàc elleducarbonediamant.Ilya8x1/8+4x1=8atomesdesiliciumparmaille.5) Calculerlerayondel'atomeenpmenconnaissantlamassevolumiquedusilicium:ρSi=2340kg.m-3.Delamassevolumique,nousendéduisonsleparamètredelamaillea:a=8.���(������)���.��� a=8∗28,1.10!!2 340.������0,5pta=542pmEtlecontactentrelesatomesdesiliciumsefaitselonlademi-diagonaledupetitcubed'arêtea/2:2���!"= 123���20,5ptrSi=117pmIIIRéductiondudioxydedesiliciumIII1)Pourproduirel esilicium,onréduitledioxydedesil iciumSiO2(s)parlecarbure decalciumCaC2(s).Pourθ<1683K,aucunchangementd'étatn'intervient.L'équationdelaréactionest:2CaC2(s)+3SiO2(s)=2CaO(s)+4CO(g)+3Si(s)Saconstanted'équilibreestnotéeK°1.6) Àl'aidedelafigure14,déterminerlesignedel'enthalpiestandardΔrH°1delaréaction(1)puissavaleurenlasupposantindépendantedelatempérature.
0,5ptApartirdelafigure14,nousremarquonsqueK°1etLnK°1sontdesfonctionscroissantesdeTet,toutnaturellement,LnK°1estunefonctiondécroissantede1/T.Nousenconcluonsquel'enthalpiestandardderéactionΔrH°1delaréaction(1)estpositive.ΔrH°1>0:(1)estuneréactionendothermique.C'estlacourbeLnK°1=f(1/T)quivanouspermettredecalculerK°1careneffet,d'après1ptlaloideVan'tHoff:������������°���������= ������°������.������quis'intègreen:LnK°1= -ΔH°!R.T+������������AinsilapentedeladroiteLnK°1=f(1/T)est-!!°!!D'aprèslesrésultatsquel'onnousfournit:-!!°!!= -125 042D'où:ΔrH°1=+125042x8,31=1039099J.mol-12ptΔrH°1=+1039,1kJ.mol-1=+1,04MJ.mol-1Laréactionesttrèstrèsendothermique.7) Quelleestl'influenced'uneaugmentationdelatempératureàpressionetcompositionconstante?Justifierclaireme ntvot reréponse.Endéduiresil'i ndustrielaintérêtàtravailleràbasseouhautetempérature.Commelaréactionestendothermique: ΔrH°1>01ptSidT>0,alorsdLnK°1>0d'aprèslaloideVan'tHoff.Conclusion:K°1augmentesiTaugmente,doncl'industrielaintérêtàtravailleràhautetempérature.8) Apartirduquotientréactionnel,préciserquelleestl'influencedelapressionPsionaugmentePàpartird'unétatinitialoùl'équilibrechimiqueestétabli.Seulelapressionvarie.
ExprimonslequotientréactionnelQ:���= (���(���������,���))!(���(������,���))!(���(������,���))!(���(���������2,���))!(���(���������2,���))!���= ���(������)���°!!11pt���= ���(������)���°������CommeCOestelseulconstituantgazeux,P(CO)=PEt:���= !!°!!Doncsil'onaugmentePtoutrestantconstantparailleurs,alorsQaugmenteetdevientdoncsupérieuràK°.danscecas,Q>K°entraîneundéplacementdel'équilibre,danslesensindirect,defaçonàcequeQdiminuedenouveaupouratteindreK°.1ptUneaugmentationdePdéplacel'équilibredanslesensindirect(<-)Figure14:courbesK°1=f(T),LnK°1=f(T),LnK°1=f(1/T)III2)Dansunréacteurdevolumeconstant8litres,préalablementvide,onintroduit18gdeSiO2(s)solideet32gdeCaC2(s)solide.Onopèreàθ=1730K>1683K.Onsupposequelaphasegazeuseestassimilableàungazparfait.9) Écrirel'équation(1')enprécisantlesétatsphysiquesdesespèceschimiques.0,5ptCommelatempératureestmaintenantsupérieureàlatempératuredefusiondusilicium,alorslesiliciumestmaintenantliquide:2CaC2(s)+3SiO2(s)=2CaO(s)+4CO(g)+3Si(l)(1')Saconstanted'équilibreestnotéeK°1'.
10) Sachantquelaconstanted'équilibredelaréaction(1')vaut:K°1(1730)=3,68.1024,calculerlapressiondusystèmesil'équilibreestatteintpuislaquantitédematièredemonoxydedecarboneformé.Conclure.Effectuonsuntableaud'avancement:18gdeSiO2=0,30mol32gdeCaC2=0,50mol1pt2CaC2(s)+3SiO2(s)=2CaO(s)+4CO(g)+3Si(l)t=00,500,30000t0,50-2ξ0,30-3ξ2ξ4ξ3ξSil'équilibreestatteint,lapressionestégaleàPéqtelleque:���°!= !é!!°!!=3,68.10241ptD'où:Péq=1,38.106bar!!!Conclusion:l'équilibrechimiquenepourrapasêtreréalisé.DePV=nRT,onendéduitlaquantitédematièredeCOàl'équilibre:���(������,é���)= 1,38.10!!.8.10!!8,31.1783���(������,é���)= 1,38.10!!.8.10!!8,31.17831ptn(CO,éq)=74510mol!!!Quantitécolossaledans8L11) Endéduirelesquantitésdematièredesdifférentesespèceschimiquesàl'étatfinal,ainsiquelapressiondelaphasegazeuse(supposéeparfaite).0,5pt Danscecas,l' état finalestun étatdanslequelilya ruptured'équilibre chimique.Recherchonsleréactiflimitant:S'ils'agitdeCaC2(s):0,50-2ξ =0lorsqueξ =0,25molS'ils'agitdeSiO2(s):0,30-3ξ =0lorsqueξ =0,10mol0,5ptLeréactiflimitantestlasiliceSiO2(s),ilrestedoncdansleréacteur:2CaC2(s)+3SiO2(s)=2CaO(s)+4CO(g)+3Si(l)t=00,500,30000t0,50-2ξ0,30-3ξ2ξ4ξ3ξtfinal0,50-2.0,10,30-3.0,12.0,14.0,13.0,1 Soit1pt0,3000,20,40,3 Lesquantitésdematièressontdoncconnues,calculonsmaintenantlapressionpartielle(maisdoncaussitotale)deCO:
���������,������������������= 0,40.8,31.17838.10!!= 74 0836 ������Soit:1,5ptP(CO,finale)=7,4barIII3)Lesiliciumobtenuestmisenréactionavecduchlorured'hydrogènegazeuxHClà300°C.OnformemajoritairementletrichlorosilaneSiHCl3maiségalementledichlorosilaneSiH2Cl2.Aprèsrefroidissementà 15°C ,onobtient unmélangeliquide deSiHCl3etdeSiH2Cl2decompositionmolaire80%enSiHCl3.UnedistillationfractionnéepermetalorsdepurifierletrichlorosilaneSiHCl3.Letrichlorosilaneultra-purestréduitparl'hydrogènevers1000°C,selonlaréaction:....SiHCl3(g)+....H2(g)=....Si(s)+....HCl(g)(2)Lesiliciumultra-pur,produitparcetteréaction,estdéposésurunbarreaudesilicium.LesiliciumobtenuestdirectementutilisablepourlafabricationdesMEMS.12) Ajusterlesnombresstoechiométriquesdel'équation(2).1pt1SiHCl3(g)+1H2(g)=1Si(s)+3HCl(g)(2)13) Quevalentà298KlesenthalpiesstandarddeformationdeH2(g)etSi(s)?0,5pt Ellessontnulles parcequecesont descorpssimplesprisdans leurétat standardderéférence.14) Calculerl'enthalpieΔrH°2delaréactionà298K.1pt D'aprèslaloideHess,ΔrH°2=ΔrH°(Si,s)+3ΔrH°(HCl,g)-ΔrH°(SiHCl3,g) -ΔrH°(H2,g)D'aprèslaloideHess,ΔrH°2=3ΔrH°(HCl,g)-ΔrH°(SiHCl3,g) ΔrH°2=211,6kJ.mol-115) LaréactionestréaliséeàlapressionP=0,1bar.Justifierlechoixdepressionégaleà0,1barplutôtque1,0baràtempératurefixée.VousutiliserezlequotientréactionnelQr.Supposonsqu'ilyaitéquilibresouslapressionP=1bar:������= ������������������������������������������������������°���Sil'onchoisitP10foisplusfaible,alorsQrdiminue,doncdevientpluspetitqueK°.Conclusion:lesystèmeévoluedanslesensdirect,cequel'onsouhaite.1ptDonccechoixesttrèsjudicieux.
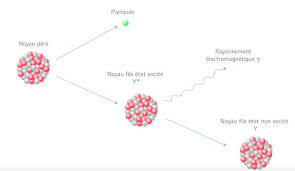
Problème2:l'uranium14ptInutiledefairedelongsdiscourspourêtreconvaincudel'importancedecetélémentchimiquedenuméroatomiqueZ=92dansnotremonde.Ainsi,aujourd'hui,laréactionnucléairedefissiondel'uraniumfournitprèsde20%delaproductiond'électricitédanslemonde.Avecplusde80%desonélectricitéproduiteparvoienucléaire,laFrancesesitueaupremierrangmondial.Cettesituation résultedechoix économiquesfaitsdanslesan nées1970etacontribuéàfairedelaFrancel'undespayspharesdansledomainedelarecherchenucléaire.Etude de quelques aspects de la chimie de l'uranium et de ses composésL'uranium,élémentradioactifnaturelquitiresonnomdelaplanèteUranus,futdécouvertenAllemagneparMartinHeinrichKlaprothen1789.Cetélément,assezrépandu,estnotammentprésentdans5%desminérauxconnusetilreprésentequelquespartiesparmilliondelacompositiondelacroûteterrestre.Ilestutilisédepuislongtempsparl'homme:ilapuparexempleêtreemployépendantdessièclescommepigmentdanslesverres.Cependant,c'estsurtoutdepuisladécouvertedelaradioactivitéàlafinduXIXèmesièclepuislamaîtriseparl'hommedesréactionsnucléairesaucoursdelapremièremoitiéduXXèmesièclequel'uraniumestdevenuunélémentstratégique,tantdupointdevueéconomique,politiquequ'écologique.Leproblèmequisuitseproposed'explorercertainsaspectsdelachimiedel'uraniumquiserévèleêtrel'unedesplusrichesconnues.URANIUMETURANINITEIL'élémentUranium1) 1,5ptleblocfestsituésouslesblocss,d,etp.Lanotation"f»désignelenombrequantiquesecondairel,quivautdoncl=3. Eneffet: l =0:électrons"sharp» l = 1 : électron p " principle » l = 2 : électron d " diffuse » l = 3 : électron f " fundamental » l = 4 : électron g,...ordre alphabétique ensuite. Ces notations ont été empruntées aux spectroscopistes. 2) Alorsallons-y,plaçons92électrons...enutilisantlarègledeKlechkowski.
2pt1s2 / 2s2 2p6 / 3s2 3p6 3d10 / 4s2 4p6 4d10 4f14 / 5s2 5p6 5d10 / 6s2 6p6 / 7s2 5f4 . Soit 86[Rn] 7s2 5f4 Rn étant le gaz rare de numéro atomique Z = 86. Remarque:Enréalité,onobserveune"anomalie"deremplissage:(Rn)7s25f36d1(nondemandéici).Lesélectronsdevalencesontceuxquisontassociésaunombrequantiqueprincipalnleplusélevé(7s2)etceuxdessous-couchesencoursderemplissage(5f4): 0,5ptL'uranium6électronsdevalence:les2électronsdel'OA7setceuxdelasous-couche5fencoursderemplissage 3) Lesdeux isotopesont92protons(Z=92)etnediffèrentque parl eurnombredeneutrons:235Uenpossède143(=235-92)et238Uenpossède146. 0,5ptDeuxisotopesayantlemêmenombredeprotons,doncd'électrons,ontlesmêmespropriétéschimiques(reliéesauxélectronsdevalence).C'estlenombredeneutronsquilesdifférencientetdoncleurnombredemasseA. IILaréductiondel'oxyded'uraniumparledihydrogène 4) Laconstanted'équilibreà1000Kétaitdonnéedansl'énoncé:CH4(g)+H2O(g)=CO(g)+3H2(g)K°(1000)=12,5.Apa rtird'untableaud' avancement,étab lissonsunbilandemati èreenpart antd'unmélangeéquimolaireenCH4etH2O: CH4H2OCOH2nTOT(gaz)Ét.initialnn002n1,5ptÉquilibren(1-η)n(1-η)nη3nη2n(1+η)Alorsd'aprèslarelationdeGuldbergetWaage:K°=PCO.PH23PCH4.PH2O⎛⎝⎜⎜⎞⎠⎟⎟éqSoitenutilisantlesfractionsmolairesetlapressionpartielledechaqueconstituant:
1ptK°=PH2P°⎛⎝⎜⎞⎠⎟3PCOP°⎛⎝⎜⎞⎠⎟PCH4P°⎛⎝⎜⎞⎠⎟PH2OP°⎛⎝⎜⎞⎠⎟=3nη2n(1+η)⎛⎝⎜⎞⎠⎟3nη2n(1+η)⎛⎝⎜⎞⎠⎟P2n(1-η)2n(1+η)⎛⎝⎜⎞⎠⎟n(1-η)2n(1+η)⎛⎝⎜⎞⎠⎟P°2=3η2(1+η)⎛⎝⎜⎞⎠⎟3η2(1+η)⎛⎝⎜⎞⎠⎟P2(1-η)2(1+η)⎛⎝⎜⎞⎠⎟(1-η)2(1+η)⎛⎝⎜⎞⎠⎟P°2K°=33.η4.P2(1-η)2.22(1+η)2.P°2=K°Pourlarésoudre,onpeutprendrelaracinedecetteéquationdedegré4etserameneràuneéquationdedegré2:K°=27.η2.P(1-η).2(1+η).P°soit:12,5=27.η22(1-η).(1+η) soit : 7,07 (1-x)(1+x) = 5,2.x2 7,07 (1-x2)= 5,2.x2 7,07 = 12,27.x2 x = 0,759 Donc,finalement,ontrouve1,5ptη≈0,76 III-RéactiondeformationdeUO2(s)àpartirdeUO3(s).5) Enthalpiestandardderéaction: UtilisonslaloideHess:ΔrH°=3ΔfH°(UO2)+3ΔfH°(H2O)-2ΔfH°(NH3)-3ΔfH°(UO3)0,5ptΔrH°=-216,5kJ.mol-10,5ptLaréactionestexothermique6) Entropiestandardderéaction:Delamêmefaçon:ΔrS°=3S°(UO2)+S°(N2)+3S°(H2O)-2S°(NH3)-3S°(UO3)0,5ptΔrS°=254,8J.K-1.mol-1 ΔrS°>0cequiétaitprévisiblecarilyaaugmentationdelaquantitédematièredegaz,doncledésordreaugmente:0,5ptΔνg>0eneffet.7) Pardéfinition:ΔrG°(T)=ΔrH°-T. ΔrS°à500KΔrG°=-343,90kJ.mol-1D'où:Constanted'équilibre:1ptK°=8,5×1035Laconstanteadoncunevaleurtrèstrèsélevéeàcettetempérature,laréactionestquantitative.8) Al'équilibre,partantuniquementdesréactifs,onremarquequel'onvaformer3foisplusd'eauquedediazote.Alorsàl'équilibre:
0,5pt3PN2=PH2O9) 3UO3(s)+2NH3(g)3UO2(S)+N2(g)+3H2O(g)K°=PH2O3.PN2PNH32.P°2K°>>1,onpeutconsidérerlaréactioncommetotale:Exprimonslapressiontotale:P=1bar=PN2+PH2O+PNH3≈PN2+PH2Ocarlaréactionétanttotale,lapressionpartielledelaquantitétrèstrèsfaibled'ammoniacrestantconduitalors,entenantcomptedurapport3entrelesdeuxpressionspartielles:1ptPN2=0,25barPH2O=0,75barUtilisonsensuiteK°pourexprimeretcalculerlapressionpartielledeNH3:1,5ptPNH3=P°.PH23PN2K= 1,2.10-19 barIV-FluorurationenUF4(s)Danslasecondemoitiédelabrancheverticaleduréacteurprécédent,l'oxydeUO2(s)rencontreunezonedefluorurationparactionàcontre-courantd'acidefluorhydriquegazeuxà700Kselonl'équilibre:UO2(s)+4HF(g)=UF4(s)+2H2O(g)K°2[2]Lapressiontotaleétantmaintenueconstante,égaleà1bar.1) Déterminerlaconstanted'équilibreK°2à700Ksilerapportdespressionspartiellesvaut,àl'équilibre:2
70HO HF P P P H 2 O 2 .P° 2 P HF 4 70
71
2 1 71
4 =70 2 .71 2
K°2=2,47.107
••• FIN •••quotesdbs_dbs1.pdfusesText_1[PDF] exercice corrigé de finance de marché
[PDF] exercice corrigé de gestion financière pdf
[PDF] exercice corrigé de la gestion de trésorerie
[PDF] exercice corrigé de macroéconomie licence 1
[PDF] exercice corrigé de macroéconomie pdf
[PDF] exercice corrigé de math financier s2
[PDF] exercice corrige de mesure
[PDF] exercice corrigé de moteur a courant continu pdf
[PDF] exercice corrigé de production de froid
[PDF] exercice corrigé de representation d'etat pdf
[PDF] exercice corrigé de topologie générale pdf
[PDF] exercice corrigé dependance fonctionnelle
[PDF] exercice corrigé diagramme d'etat de transition uml pdf
[PDF] exercice corrigé dipole rc bac technique
