 Chapitre CHIMIE – Le pH I – Les solutions acides neutres et
Chapitre CHIMIE – Le pH I – Les solutions acides neutres et
□ Ions hydroxyde □ Ions hydrogène □ Ions phosphate □ Ions citrate □ Ions acétate Document n°3 : Tableau récapitulant les réactifs permettant d'identifier ...
 Cours - Atomes - Ions - Molecules.pdf
Cours - Atomes - Ions - Molecules.pdf
24 janv. 2020 Un ion monoatomique est une entité chimique stable dont la couche de valence est saturée. La position de l'élément dans le tableau périodique ...
 Fiche de révision de 3eme en physique chimie - DNB
Fiche de révision de 3eme en physique chimie - DNB
Une solution ionique s'écrit : (ion+ + ions -). Exemples : sulfate de cuivre (Le tableau suivant n'est pas à apprendre). Ion. Chlorure. Cl-. Cuivre. Cu2+. Fer ...
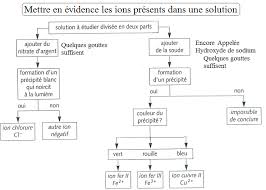 Chapitre CHIMIE – Comment identifier les IONS présents dans une
Chapitre CHIMIE – Comment identifier les IONS présents dans une
NEGATIFS....... 2) Par exemple dans une solution Ionique de Chlorure de Sodium (eau salée) il y a des Ions .CHLORURES...
 Exercices de révisions : Physique-chimie
Exercices de révisions : Physique-chimie
Initialement le système chimique contient 30 mol de diiode et 5
 Chapitre 2 24 Titrage des ions bromure 1. On a le tableau d
Chapitre 2 24 Titrage des ions bromure 1. On a le tableau d
24 Titrage des ions bromure. 1. On a le tableau d'avancement : Équation de la réaction. 6 Br– (aq) + Cr2 7. 2− (aq) + 14 H+ (aq) → 3 Br2 (aq) + 2. Cr3+ (aq)
 QUELQUES TESTS DIDENTIFICATION DES IONS
QUELQUES TESTS DIDENTIFICATION DES IONS
TABLEAU RECAPITULATIF DES TESTS D'IDENTIFICATION DES IONS. Réactif utilisé Si des ions chlorures sont présents alors il se forme un précipité blanc qui ...
 Physique Chimie
Physique Chimie
Document 3 -. Tableau d'identification des ions. Un précipité est un solide formé par la réaction entre deux ions dissous. Ion à identifier. Réactif test.
 Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques. Formules. Constantes et conversions. Solubilité des composés ioniques dans l'eau à 25 °C. Ions -. 1. Ions -. 2. Ions -.
 Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques. Formules. Constantes et conversions. Solubilité des composés ioniques dans l'eau à 25 °C. Ions -. 1. Ions -. 2. Ions
 Exercices de révisions : Physique-chimie
Exercices de révisions : Physique-chimie
Exercice n°2 : Quantité de matière et tableau d'avancement Calculer la concentration finale en ions I?-?(aq) dans le mélange si le volume total à.
 Le tableau périodique simplifié des éléments
Le tableau périodique simplifié des éléments
d'ions hydroxyde que d'ions calcium car la charge totale doit être égale à 0. Page 7. Répétition 2e. AdM. 7. Les substances chimiques.
 Chapitre 2 24 Titrage des ions bromure 1. On a le tableau d
Chapitre 2 24 Titrage des ions bromure 1. On a le tableau d
24 Titrage des ions bromure. 1. On a le tableau d'avancement : Équation de la réaction. 6 Br– (aq) + Cr2 7. 2? (aq) + 14 H+ (aq) ? 3 Br2 (aq) + 2.
 tableau davancement
tableau davancement
Quelle est la concentration finale en ions HO— s'il n'y a pas de variation du volume ? On commence par calculer les quantités de matière des espèces introduites
 Tableau récapitulatif des principaux ions de la chimie. CATIONS
Tableau récapitulatif des principaux ions de la chimie. CATIONS
On peut alors savoir les ions présents lors de la dissolution d'un composé ionique dans l'eau : Sulfate de cuivre : CuSO4 qui donne dans l'eau les ions Cu2+.
 ELECTROPHYSIOLOGIE: PRINCIPES ET TECHNIQUES
ELECTROPHYSIOLOGIE: PRINCIPES ET TECHNIQUES
Tableau 1: Concentrations [Ion]
 Chapitre VI: Lévolution des réactions chimiques
Chapitre VI: Lévolution des réactions chimiques
exemple: les ions iodure I - avec les ions peroxodisulfate S2O8 espèce n°1: ions iodure ... 4/ Le tableau d'évolution (ou tableau d'avancement).
 QUELQUES TESTS DIDENTIFICATION DES IONS
QUELQUES TESTS DIDENTIFICATION DES IONS
QUELQUES TESTS D'IDENTIFICATION DES IONS. TABLEAU RECAPITULATIF DES TESTS D'IDENTIFICATION DES IONS. Réactif utilisé. Hydroxyde de sodium ou soude. Nitrate.
 LES IONS CATIONS ANIONS
LES IONS CATIONS ANIONS
LES IONS. CATIONS. FORMULES. ANIONS. FORMULES ion oxonium. H3O + ion hydroxyde. HO - ion cuivre II. Cu 2+ ion nitrate. NO3. - ion sodium. Na + ion iodure.
 [PDF] Tableau de certains ions polyatomiques Formules Constantes et
[PDF] Tableau de certains ions polyatomiques Formules Constantes et
Tableau de certains ions polyatomiques Formules Constantes et conversions Solubilité des composés ioniques dans l'eau à 25 °C Ions - 1 Ions - 2 Ions
 [PDF] LES IONS CATIONS ANIONS
[PDF] LES IONS CATIONS ANIONS
LES IONS CATIONS FORMULES ANIONS FORMULES ion oxonium H3O + ion hydroxyde HO - ion cuivre II Cu 2+ ion nitrate NO3 - ion sodium Na + ion iodure
 Nomenclature inorganique : liste des principaux ions
Nomenclature inorganique : liste des principaux ions
Ion Al3+ aluminium Ag+ argent Ba2+ baryum Ca 2+ calcium Cd 2+ cadmium Co 2+ cobalt (II) Cr 3+ chrome (III) Cu+ cuivre (I)
 [PDF] ionspdf
[PDF] ionspdf
Structure électronique de l'ion Demi équation électronique Struct elec Gain ou perte d'e Formule ion Compléter les tableaux suivants atome Na (Z=11)
 [PDF] Tableau récapitulatif des principaux ions de la chimie
[PDF] Tableau récapitulatif des principaux ions de la chimie
Tableau récapitulatif des principaux ions de la chimie CATIONS ANIONS ions portant une seule charge H + proton H3O + ion hydronium NH4 + ion
 [PDF] Le tableau périodique simplifié des éléments
[PDF] Le tableau périodique simplifié des éléments
d'ions hydroxyde que d'ions calcium car la charge totale doit être égale à 0 Page 7 Répétition 2e AdM 7 Les substances chimiques
 [PDF] les atomes molécules et ions - La chimie
[PDF] les atomes molécules et ions - La chimie
Atomes molécules et ions tableau dans lequel sont regroupés les un ion est un atome ou une molécule qui a gagné ou perdu des électrons
 [PDF] Leçon 2 : atomes et ions Physique chimie
[PDF] Leçon 2 : atomes et ions Physique chimie
Ion hydrogène 0 Exercice n°5 : Charge et formule de quelques ions Complétez le tableau (correction à la fin du diaporama)
 [PDF] QUELQUES TESTS DIDENTIFICATION DES IONS
[PDF] QUELQUES TESTS DIDENTIFICATION DES IONS
TABLEAU RECAPITULATIF DES TESTS D'IDENTIFICATION DES IONS Si des ions chlorures sont présents alors il se forme un précipité blanc qui noircit à la
LES IONS
CATIONS FORMULES ANIONS FORMULES
ion oxonium H 3 O ion hydroxyde HO ion cuivre II Cu 2+ ion nitrate NO 3 ion sodium Na ion iodure I ion calcium Ca 2+ ion fluorure F ion ferreux ou fer II Fe 2+ ion bromure Br ion ferrique ou fer III Fe 3+ ion chlorure Cl ion argent Ag ion hypochlorite ClO ion magnésium Mg 2+ ion sulfate SO 4 2- ion potassium K ion hydrogénosulfate HSO 4 ion plomb Pb 2+ ion carbonate CO 3 2- ion ammonium NH 4 ion hydrogénocarbonate HCO 3 ion zinc Zn 2+ ion phosphate PO 4 3- ion aluminium Al 3+ ion hydrogénophosphate HPO 4 2- ion chrome Cr 3+ ion dihydrogénophosphate H 2 PO 4 ion cobalt II Co 2+ ion permanganate MnO 4 ion cobalt III Co 3+ ion carboxylate R - COO ion étain Sn 2+ ion dichromate Cr 2 O 7 2- ion sulfure S 2- ion thiosulfate S 2 O 3 2- ion peroxodisulfate S 2 O 8 2- ion tetrathionate S 4 O 6 2-MOLECULES et COMPOSES IONIQUES
MOLECULES FORMULES
COMPOSES
IONIQUES
FORMULES
dioxygène O 2 (g) hydroxyde de sodium (soude) NaOH dihydrogène H 2 (g) chlorure de sodium (sel) NaCl diazote N 2 (g) sulfate de cuivre CuSO 4 dichlore Cl 2 (g) nitrate d'argent AgNO 3 dibrome Br 2 (L) chlorure d'argent AgCl diiode I 2 (s) hydroxyde de potassium (potasse) KOH méthane CH 4 (g) permanganate de potassium KMnO 4 dioxyde de carbone (gaz carbonique) CO 2 (g) dichromate de potassium K 2 Cr 2 O 7 monoxyde de carbone CO (g) dioxyde d'azote NO 2 (g) ammoniac NH 3 (g) ammoniaque NH3 (aq)
eau H 2 O (L) glucose C 6 H 12 O 6 (s) saccharose (sucre) C 12 H 22O
11 (s)
acide carbonique CO2 (aq)
, H 2 O acide éthanoïque (acétique) CH 3 - COOH (L) peroxyde d'hydrogène (eau oxygénée) H 2 O 2 (L) benzène C 6 H 6 (L) acide benzoïque C 6 H 5 - COOH (s) glycérol CH 2OH-CHOH-CH
2 OHLES FAMILLES de MOLECULES
éthane CH
3 - CH 3LES ALCANES C
n H 2n+2 propane CH 3 - CH 2 - CH 3éthène (éthylène) CH
2 = CH 2LES ALCENES C
n H 2n but-1-ène CH 2 = CH - CH 2 - CH 3éthanol (primaire) CH
3 - CH 2 - OH propan-2-ol (secondaire) CH 3 - CHOH - CH 3LES ALCOOLS R - OH
méthylpropan-2-ol (tertiaire) HO - C ( CH 3 3éthanal CH
3 - CHOLES ALDEHYDES R - CO - H
propanal CH 3 - CH 2 - CHOLES CETONES R - CO - R' propanone (acétone) CH
3 - CO - CH 3 acide méthanoïque (formique) H - COOHACIDES CARBOXYLIQUES R - CO - O - H
acide éthanoïque (acétique) CH 3 - COOH méthylamine (primaire) CH 3 - NH 2éthyl-méthylamine (secondaire) C
2 H 5 - NH - CH 3LES AMINES R - NH
2 triméthylamine (tertiaire) N(CH 3 3 LES ESTERS R - CO - O - R' éthanoate de méthyle C 2 H 5 - COO - CH 3 ANHYDRIDES D'ACIDES R- CO - O - CO - R'anhydride acétique CH 3 -CO - O - CO-CH 3HCl / Cl
chlorure d'hydrogène / ion chlorure HNO 3 / NO 3 acide nitrique / ion nitrate H 2 SO 4 / HSO 4 acide sulfurique / ion hydrogénosulfate H 3 PO 4 / H 2 PO 4 acide phosphorique / ion dihydrogénophosphateACIDES
NON-ORGANIQUE
CO2 (aq)
, H 2O / HCO
3 acide carbonique / ion hydrogénocarbonateLES TESTS de RECONNAISSANCE
ESPECES CHERCHEES REACTIFS OBSERVATIONS EN CAS DE TEST POSITIF O 2 bûchette incandescente le dioxygène ravive l'incandescence H 2 flamme petite détonation ( le dihydrogène brûle ) CO 2 eau de chaux l'eau de chaux se trouble au contact du gaz carbonique H 2 O sulfate de cuivre anhydre solide blanc qui devient bleu au contact de l'eau Lumière AgCl solide blanc qui devient noir à la lumière acidité papier pHquotesdbs_dbs6.pdfusesText_12[PDF] population france 1945
[PDF] population en france en 2017
[PDF] comment élever des poules pondeuses pdf
[PDF] comment nourrir poules pondeuses
[PDF] elever des poules pour les nuls pdf
[PDF] frequence respiratoire en fonction de l'age
[PDF] fréquence cardiaque adulte
[PDF] fréquence respiratoire personne agée
[PDF] normes paramètres vitaux oms
[PDF] fréquence respiratoire normes
[PDF] norme fréquence cardiaque
[PDF] comment mesurer la fréquence respiratoire
[PDF] frequence respiratoire norme
[PDF] frequence cardiaque en fonction de l'age
