 Conductance et conductivité
Conductance et conductivité
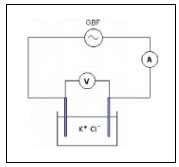
Exercice 1 : La mesure de la conductivité d'une solution de chlorure de potassium + + − de concentration C.
 LA CONDUCTIMÉTRIE
LA CONDUCTIMÉTRIE
EXERCICES. Partie 1/ Chimie minérale. Fiche 8 : Conductimétrie. Quelques ions avec leur conductivité molaire ionique en S.m2.mol-1. Cuivre. Fer 2. Sodium.
 Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Justifier votre réponse. ACCÈS CORRECTION. Extrait 8 : Bac S 2014 Pondichéry http://labolycee.org. Exercice Le titrage est suivi par conductimétrie. Le volume ...
 Solution de Exercices de La conductance et la conductivité
Solution de Exercices de La conductance et la conductivité
2) les facteurs qui influencent la conductivité sont : -- la température de la solution. -- la concentration (C) de la solution ionique. Exercice_4. On veut
 Cours de soutien Conductance et conductivité 1BAC Fr. Bac
Cours de soutien Conductance et conductivité 1BAC Fr. Bac
Quelle est la valeur de la conductance G ? Exercice 4 : Conductance et conductivité molaire ionique : 1) La conductance d'une solution de chlorure de sodium
 Chapitre 2 – Analyse dun système Exercices supplémentaires
Chapitre 2 – Analyse dun système Exercices supplémentaires
Une sonde conductimétrique est immergée dans une solution ionique de chlorure de potassium. (K+(aq) Cl–(aq)). La conductance mesurée est de 5
 Exercices : corrigé
Exercices : corrigé
On veut suivre l'évolution de la réaction par conductimétrie. On rappelle que la conductivité s de la solution est donnée par l'expression : = °i.Ci i. Où
 Terminale générale - Méthodes danalyse physique - Exercices
Terminale générale - Méthodes danalyse physique - Exercices
m-1. Déterminer la conductivité d'une solution à 10-3mol.L-1 de KOH. (K++OH-). Exercice 6 corrigé disponible. Dans les mêmes conditions expérimentales on
 Ch.18. Exercice corrigé p : 479 n°10. CONTRÔLE DE QUALITE PAR
Ch.18. Exercice corrigé p : 479 n°10. CONTRÔLE DE QUALITE PAR
La concentration en ions chlorure varie-t-elle au cours du titrage? c. L'expression de la conductivité σ de la solution contenue dans le bécher est : σ = λ(H3O+)
 1ére bac SMF Mahdade Allal année scolaire 2015-2016
1ére bac SMF Mahdade Allal année scolaire 2015-2016
CONDUCTION DANS LES SOLUTIONS : exercices. Choisir la (ou les) bonne(s) À partir des conductances mesurées déterminer la conductivité σ des solutions 1
 Conductance et conductivité
Conductance et conductivité
Exercice 1 : La mesure de la conductivité d'une solution de chlorure de potassium + + ? de concentration C.
 Exercices : corrigé
Exercices : corrigé
Où Ci est la concentration de l'ion i exprimée en mol.L-1 et ?i° la conductivité molaire à dilution infinie de l'ion i. ?i° est propre à chaque ion.
 Travaux dirigés : Conductance et Conductivité
Travaux dirigés : Conductance et Conductivité
Le corrigé des exercices du livre indiqués sur la feuille est aussi sur le Une cellule conductimétrique est constituée de deux électrodes de surface S ...
 Ch.18. Exercice corrigé p : 479 n°10. CONTRÔLE DE QUALITE PAR
Ch.18. Exercice corrigé p : 479 n°10. CONTRÔLE DE QUALITE PAR
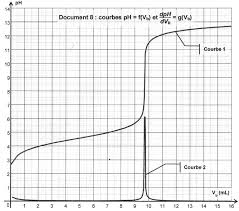
Justifier l'évolution de la conductivité. On dose par titrage conductimétrique
 Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
Dosages par titrage direct 10 Extraits de sujets corrigés du bac S
métrique conductimétrique et par pente dans un titrage conductimétrique. ... EXERCICE 2 – UN EXEMPLE DE CHIMIE VERTE : LA SYNTHÈSE DE L'IBUPROFÈNE.
 Cours de soutien Conductance et conductivité 1BAC Fr. Bac
Cours de soutien Conductance et conductivité 1BAC Fr. Bac
Exercice 4 : Conductance et conductivité molaire ionique : 1) La conductance d'une solution de chlorure de sodium de concentration C1= 0
 Conductance et conductivité dune solution ionique
Conductance et conductivité dune solution ionique
exercices corrigés. À l'aide d'un conductimètre on mesure la conductivité ? = 4
 Terminale générale - Méthodes danalyse physique - Exercices
Terminale générale - Méthodes danalyse physique - Exercices
Exercice 3 corrigé disponible. On plonge une cellule de conductimétrie dans une solution pour mesurer sa conductivité ? . 1. Réaliser le schéma du montage
 Suivi temporel dune transformation chimique vitesse de réaction
Suivi temporel dune transformation chimique vitesse de réaction
Exercices corrigés. Exercice 1 : 7- La réaction précédente peut-être suivie en mesurant la conductivité de la solution en fonction du.
 Chapitre 2 – Analyse dun système Exercices supplémentaires
Chapitre 2 – Analyse dun système Exercices supplémentaires
Une sonde conductimétrique est immergée dans une solution ionique de chlorure de potassium. (K+(aq) Cl–(aq)). La conductance mesurée est de 5
 [PDF] Conductance et conductivité - AlloSchool
[PDF] Conductance et conductivité - AlloSchool
Exercice 1 : La mesure de la conductivité d'une solution de chlorure de potassium + + ? de concentration C donne 1224 ?1 à 21°C
 [PDF] Travaux dirigés : Conductance et Conductivité
[PDF] Travaux dirigés : Conductance et Conductivité
Travaux dirigés : Conductance et Conductivité * Le corrigé des exercices du livre indiqués sur la feuille est aussi sur le site du lycée *
 [PDF] Corrigés des exercices sur la conductimétrie
[PDF] Corrigés des exercices sur la conductimétrie
Corrigés des exercices sur la conductimétrie 6 page 69 8 page 70 a La conductance G est proportionnelle à la conductivité ?elle même proportionnelle la
 [PDF] ex08conductimetriepdf
[PDF] ex08conductimetriepdf
EXERCICES Partie 1/ Chimie minérale Fiche 8 : Conductimétrie Quelques ions avec leur conductivité molaire ionique en S m2 mol-1
 [PDF] Exercices : corrigé
[PDF] Exercices : corrigé
Où Ci est la concentration de l'ion i exprimée en mol L-1 et ?i° la conductivité molaire à dilution infinie de l'ion i ?i° est propre à chaque ion
 Telecharger 08conductimetrie-correctionpdf pdf examens corriges
Telecharger 08conductimetrie-correctionpdf pdf examens corriges
CORRECTION EXERCICES Partie 1/ Chimie minérale Fiche 8 : Conductimétrie Quelques ions avec leur conductivité molaire ionique en S m2 mol-1
 [PDF] solution-de-exercices-de-la-conductance-et-la-conductivitc3a9pdf
[PDF] solution-de-exercices-de-la-conductance-et-la-conductivitc3a9pdf
1 2) La conductivité d'une partie d'une solution électrolytique dépend de la tension appliquée aux électrodes et au courant électrique qui passe dans le
 [PDF] Ch18 Exercice corrigé p : 479 n°10 CONTRÔLE DE QUALITE PAR
[PDF] Ch18 Exercice corrigé p : 479 n°10 CONTRÔLE DE QUALITE PAR
EXERCICE p : 479 n°10 Justifier l'évolution de la conductivité On dose par titrage conductimétrique une solution SA d'acide chlorhydrique H3O+
 [PDF] correction exercices de revision : conductivite des solutions - PC-STL
[PDF] correction exercices de revision : conductivite des solutions - PC-STL
CORRECTION EXERCICES DE REVISION : CONDUCTIVITE DES SOLUTIONS Exercice 1 (D'après BTS BIOTECHNO 2002 Conductivité Composé peu solubles)

FŃPMŃ P ŃŃPP Exercice 1 : IM M ŃŃPP P ŃO PM de concentration C donne -- 21FB 1- Exprimer M ŃŃPP . 2- On donne les valeurs suivantes : ; 2B1 P M PP ? 2.2) Donnes ces valeurs en . 2-3 M ŃŃPMP en . Correction 1- IM ŃŃPP est : -- - - -- ------ --- 2.1) la lettre P M ŃŃPP M s chlorure et des ions potassium . 2B2 IM ŃŃPP M est de : - IM ŃŃPP M est de : - 2.3) la concentration : Puisque : alors :
----- - - Exercice 2 : 1-FŃPMŃ P ŃŃPP : Ń ŃŃPP P ŃPP PMP M PM MŃ -- . 1.1- Calculer le rapport . 1.2- On mesure une conductance - P ŃPP B FMculer la ŃŃPP ŃMP ŃMP P PB 2- FŃPP P ŃŃPP M : Une solution de chlorure de potassium a une concentration - . 2.1- Ecrire MP M MŃP P M M ŃO PMB 2.2- La dissolution est totale. Calculer, en , les concentrations dans la solution des ions et P ŃMP P B 2.3- FMŃ M ŃŃPP M PB ŃŃPP M : - et - Correction 1.1- Rapport : -- 1.2- IM ŃŃPP : ---- -- 2.1-MP M MŃP P de M M :
2.2- Les concentrations dans la solution des ions et : La dissolution est totale : A.N : - - - -- 2.3- IM ŃŃPP : --- Exercice 3 : 1- M Ń P M ŃŃPMŃ P 1 de chlorure de sodium de concentration - ; on trouve - 1.1- Ecrire MP M MŃP ŃMP ŃO M MB 1.2- La dissociation de est totale. GP ŃŃPMP puis en des ions et B IM M ŃMP ÓPB 1.3-GP M ŃŃPP M PB On donne ŃŃPP M : - - 1.4- (L PMŃ P ŃP, S sMŃ ŃP) est appel constante de la cellule B GP B 2- On dilue 10 fois la P ŃP P ) : On appelle la solution obtenue. 2.1- MP PP NP 100I MP M P . 2.2- P M ŃŃPMP Ń P M M P ? On utilise la Ń ŃŃPP ŃP pour mesurer la conductance de la solution 2.3- GPr la conductance de la solution . 2.4- IM P M N M Ń P M P 1B FMŃ PP H ŃMP PM M Ń P M ŃPB ŃŃPP M : - -
Correction 1.1- MP M MŃP 1.2- Les concentrations des ions et : IM ŃMP PMP PPM une mole de P MP et une M M P P M ŃP : - -- - -- 1.3- M ŃŃPP M P : --- 1.4- GPMP : --- 2.1- MP P NP 100I : P M N P PP : M -- de solution fille de concentration MP - P B 10I MŃ PP ÓM M ÓM 100I, on verse de M P ÓM PMP ÓMB On agite pour obtenir une solution OB 2.2- ŃŃPMP Ń : P ŃŃPMP P M 10 :
-- - -- - 2.3- La conductance de la solution : La conductance est aussi par 10 : - 2.4- IPP H ŃMP : -- Exercice 4 : N Ń M P ŃO PM P NMŃO MP MPMP M P ŃMŃ P PP ŃMŃ . 1- FMŃ M PMŃ M P ŃPP Ń P ŃPB 2- Calculer la conductance en S. 3- IM ŃŃPP ŃPP P P -- -- . Calculer la valeur de la constance k de cette cellule. Correction 1- IM PMŃ : - 2- La conductance : - 3- La constance k de la cellule :
----- Exercice 5 : IOM ŃMŃ M P PM ; pour compenser rapidement cette carence, on peut utiliser une solution de chlorure de potassium, qui se trouve dans une ampoule de -- contenant de B Piner cette masse P PM ŃO PM - P PM ŃŃPPB 1- PM M Ń ŃŃPP M MP M P PM , cinq solutions filles de volume -- et de concentrations respectives - ; - ; - ; -- et - . C() - -- - - - -- G(mS) -- - - -- - Tracer la courbe M PMNM Ń-dessus. Conclure. 2.1- M MŃ Ń PM P M PMP ; la conductance de la solution de MB NPP : - . Peut- P ŃPP M ŃŃPMP ŃO potass M Ń ŃPP ŃN P M B 2.2- Compte tenu des valeurs de - et - , quel est le facteur minimal de dilution P ? 3- I ŃP M M P 200 B IM M ŃŃPMŃ : B M M M ŃŃPMP M P Ń la solution MB FMŃ M M B G : ; Correction 1- la courbe :
2.1- Peut- P ŃPP M ŃŃPMP ŃO PM M Ń cette courbe ? IM M ŃŃPMŃ P O ŃN PMMB MP M ŃN PMM M MP M ŃP ŃP ŃPP ŃN P ŃŃPMPB On ne pa Ń ŃPP M concentration de la solution. M P MP MŃP P Ń Mre la mesure M ŃŃPP M ŃŃPMP M P P M ŃŃPMP M P MPB Remarque : - IM ŃŃPMŃ P P M ŃŃPP elle- P M concentration. - I MŃP PMP P 36 : -- 2.2- le facteur de dilution : En divisant par 100 la conductance (ŃP--dire en diluant par 100) on pourra utiliser la courbe PMMB 3- La masse m : Pour une mesure de on obtient : IM P MP P 200 ŃŃP ŃP--dire --- ---- La concentration de M M P Ń Le nombre de mole de M M -- est de : ----- La masse de M M P :
--- Exercice 6 : M un volume --- de solution de chlorure de potassium ) concentration -- et un volume -- de solution de chlorure de sodium ( concentration -- . 1- P M ŃŃPP M P NP ? 2- GM M ŃP MŃ M Ń ŃŃPPB IM MŃ ŃP P de - et la PMŃ MP P . Quelle est la valeur de la conductance ? ŃŃPP M : -- - - Correction 1- IM ŃŃPP M : H MP P MN MPP MP M M P ŃMŃ P M concentration de chaque ion. --------- ------- - ----- ----- ---- ----- ------- 2- La valeur de la conductance :
------ Exercice 7 : Une cellule conductimétrique est constituée de deux électrodes de surface spares dune distance - et soumises à une tension continue - . La cellule est plongée dans une solution ionique lintensit du courant traersant la cellule mesure - . 1- Exprimer et calculer la conductance et la résistance de la cellule. 2- Exprimer et calculer k la constante de la cellule en et . 3- Exprimer et calculer la conductivité en unité S.I. 4- La solution ionique a une concentration - . Exprimé la concentration en unité , et calculer la conductivité molaire de la solution. Correction 1- Exprimons et calculons la conductance et la résistance de la cellule : ---- ---- 2- Exprimons et calculons k la constante de la cellule en et : -- - 3- Exprimer et calculer la conductivité : --- 4- Exprimons la concentration en unité : - -- -- Calculons la conductivité molaire de la solution : - - -
Exercice 8 : La solution de nitrate de calcium est formée des ions de calcium et des ions nitrates hydratés. 1- Ecrire luation de la raction de la dissolution de nitrate de calcium dans leau. 2- On dispose dune solution aueuse de nitrate de calcium de concentration massique . Déterminer la concentration molaire apportée et les concentrations molaires des ions dans la solution. 3- Déterminer la conductivité de la solution à 25°C. 4- Déduire la conductivité de la solution. Données à 25°C : - ; Correction 1- luation de la raction de la dissolution : - 2- La concentration molaire apportée : Avec ----- - Les concentrations molaires des ions dans la solution : - -- 3- la conductivité de la solution : ---- 4- La conductivité molaire de la solution : --
--- Exercice 9 : La conductivité à dune solution sature de fluorure de calcium est de . Déduire la concentration molaire des ions dans la solution et la solubilité du fluorure de calcium à . Données à 18°C : -- ; - Correction Equation de dissolution de dans leau : - - Concentration apportée de -- - ----------- --- Exercice 10 : On plonge les lectrodes dune cellule dun conductimtre dans une solution aueuse de chlorure de potassium. On applique aux bornes des électrodes une tension alternative sinusoïdale. Les valeurs efficaces de la tension est et de lintensit du courant est . 1- Représenter le montage expérimental utilisé. 2- Calculer la conductance G de la portion dlectrolyte comprise entre les lectrodes 3- La conductivité de cette solution est égale à - calculer la constante de la cellule. 4- Si les électrodes, planes et parallèles, sont séparées de 1cm, quelle est leur surface. Correction
1- Le montage expérimental utilisé : (voir figure ci-contre) 2- La conductance G de la portion dlectrolyte comprise entre les électrodes : --- - 3- La constante de la cellule : ------ 4- La surface S de llectrode : -- Exercice 10 : 1- On prépare deux solutions aqueuses diluées : la première solution en dissolvant le chlorure de sodium et le deuxième en dissolvant le chlorure de baryum . 1-1- Ecrire la formule de chaque solution. 1-2- Exprimer la conductivité de chaque solution en fonction de la concentration molaire. 2- On dispose dune solution dacide nitriue de conductivité -- . Calculer la concentration molaire de cette solution. On donne les conductivités molaires ioniques : - ; Correction 1- On prépare deux solutions aqueuses diluées : 1-1- La formule de chaque solution : Luation de la raction de dissolution de chlorure de sodium :
Formule de la première solution : ( Luation de la raction de dissolution de chlorure de baryum : Formule de la deuxième solution : ( 1-2- La conductivité de chaque solution en fonction de la concentration molaire : Solution de chlorure de sodium : Concentration apportée de Solution de de chlorure de baryum : - Concentration apportée de -- 2- La concentration molaire de cette solution La conductivité de la solution : ---- - Exercice 11 :
A laide dune cellule, on dtermine la conductance dune portion de solution de chlorure de sodium de concentration - ; on trouve - . 1- Calculer la conductivité de la solution de chlorure de sodium. 2- Calculer la constante de la cellule utilisée. On donne les conductivités molaires ioniques : -- ; Correction 1- Calcul de la conductivité : A.N : ---- soit : -- 2- Calcul de la constante de cellule : -- -- Exercice 12 : Dans les mêmes conditions expérimentales, on a mesuré les conductances de trois solutions aqueuses de mémé concentration - ; et on a trouvé : *--- pour la solution dacide chlorhydriue ; *- pour la solution dacide sulfuriue - ; *- pour la solution de sulfate de cuivre . Trouer la conductance dune portion de la solution de chlorure de cuivre - de même concentration et de mêmes conditions expérimentales identiques. Correction La conductivité de la solution dacide chlorhydriue
La conductance de la solution La conductivité de la solution dacide sulfuriue - - - - La conductance de la solution - - - La conductivité de la solution de sulfate de cuivre La conductance de la solution Pour obtenir la solution de chlorure de cuivre - cest-à-dire - -- -- - - -------
quotesdbs_dbs2.pdfusesText_2[PDF] conductimétrie formule
[PDF] conductimétrie pdf
[PDF] conductivité de l'eau potable
[PDF] facteur de correction température conductivité
[PDF] influence de la température sur la conductivité de l'eau
[PDF] conversion conductivité salinité
[PDF] conversion ms/cm en g/l
[PDF] conductivité en fonction de la température
[PDF] la conductivité d'une solution
[PDF] mesure de conductivité d'une solution
[PDF] relation conductivité température
[PDF] facteur de correction conductivité
[PDF] conductivité eaux usées domestiques
[PDF] cours conductivité électrique pdf
