CRISTALLOGRAPHIE
CRISTALLOGRAPHIE
PLAN DU COURS. I L'état cristallin. 1) Solides amorphes et solides cristallins. 2) Le modèle du cristal parfait. 3) Définitions fondamentales de
 cristallographie 2a mp 2016
cristallographie 2a mp 2016
plan du cours de structure de la matière révision du cours de première année. ÉTUDE DE LA MATIÈRE À L'ÉTAT SOLIDE. I) GÉNÉRALITÉS SUR LA MATIÈRE À L'ÉTAT
 COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
COURS DE CHIMIE-PCSI/MPSI/TSI- elfilalisaid@yahoo.fr Page -2
me ≃ 1836 ( c'est à dire la masse des électrons est très négligeable devant celle des nucleons). 7. Page 7. 1.1. RAPPEL. COURS DE CHIMIE-PCSI/MPSI
 Chapitre 5 :Systèmes cristallins
Chapitre 5 :Systèmes cristallins
I Vocabulaire de la cristallographie. A) Solide cristallin. Solide : Les constituants https://www.immae.eu/cours/. Page 2. Chapitre 5 : Systèmes cristallins.
 CRISTALLOGRAPHIE
CRISTALLOGRAPHIE
MPSI 2. Exercices de Chimie 2019-20. CRISTALLOGRAPHIE. Donnée : NA = 602.1023 mol-1. N°1 : Alliage or-argent. L'argent de rayon atomique rAg = 144 pm
 Cristallographie minéralogie
Cristallographie minéralogie
https://ipag.osug.fr/~beckp/Research/Teaching_files/mineralo_CAPES_2010.pdf
 Cristallographie
Cristallographie
motifs que contient cette maille : Le nombre de motifs que. Règles Un motif opportemont à compte. Ex : en. * Cutique: Chaque motif (8) apportiat à 8 mailles.
 Programme de Chimie 2ème année Sections MP-T et PC
Programme de Chimie 2ème année Sections MP-T et PC
Thème 1 : Cristallographie Cependant la progression retenue au cours d'un semestre doit respecter les objectifs de l'enseignement dispensé au cours de cette ...
 [PDF] Chapitre 4 : Cristallographie - Free
[PDF] Chapitre 4 : Cristallographie - Free
Chapitre 4 : Cristallographie I Généralités sur l'état solide ? Solides cristallins et solides amorphes modèle du cristal parfait
 [PDF] Plan du cours Cristallographie - Chimie en PCSI
[PDF] Plan du cours Cristallographie - Chimie en PCSI
Un cristal est un arrangement triplement périodique d'atomes d'ions ou de molécules 2014 Année Internationale de la Cristallographie Premier chapitre de l'
 [PDF] Chapitre 5 :Systèmes cristallins - Melusine
[PDF] Chapitre 5 :Systèmes cristallins - Melusine
I Vocabulaire de la cristallographie A) Solide cristallin Solide : Les constituants élémentaires 4 0 International” https://www immae eu/cours/
 [PDF] cristallographie 2a mp 2016 - Unisciel
[PDF] cristallographie 2a mp 2016 - Unisciel
plan du cours de structure de la matière révision du cours de première année définition : on appelle site interstitiel ou cristallographique une cavité
 [PDF] Cours CH3 Solides cristallins - Thierry FERRARI
[PDF] Cours CH3 Solides cristallins - Thierry FERRARI
MPSI – 2018-2019 – Lycée Jeanne d'Albret D Malka CH3 – Solides cristallins 1 3 Le modèle du cristal parfait Dans la suite du cours nous décrivons la
 [PDF] Poly-13x14-Cristallographiepdf - Physique-Chimie – BCPST
[PDF] Poly-13x14-Cristallographiepdf - Physique-Chimie – BCPST
On ne s'intéressera dans ce cours qu'à l'état cristallin et plus particulièrement au modèle du cristal parfait dans lequel la périodicité est parfaite
 [PDF] Solides cristallins - Étienne Thibierge
[PDF] Solides cristallins - Étienne Thibierge
11 déc 2017 · 4 - Définir et calculer la compacité C de la structure cubique centrée Exercice 2 : Galène [?00] L'élaboration du plomb par voie sèche
 [PDF] TD : Cristallographie Enoncés et éléments de réponses
[PDF] TD : Cristallographie Enoncés et éléments de réponses
TD : Cristallographie Structure du carbone solide (mines MP 2006) Structure cristalline du fer et de l'acier ( E3A MP 2008 )
 [PDF] CRISTALLOGRAPHIE - Chimie - PCSI
[PDF] CRISTALLOGRAPHIE - Chimie - PCSI
Page 1 sur 30 CRISTALLOGRAPHIE PLAN DU COURS I L'état cristallin 1) Solides amorphes et solides cristallins 2) Le modèle du cristal parfait
 [PDF] Chapitre 4 : Cristallographie - Free
[PDF] Chapitre 4 : Cristallographie - Free
La cristallographie est l'étude des solides cristallins ou « cristaux » On se limite aux solides cristallins dont l'organisation sera supposé parfaitement
 [PDF] Chapitre 5 :Systèmes cristallins - Melusine
[PDF] Chapitre 5 :Systèmes cristallins - Melusine
I Vocabulaire de la cristallographie A) Solide cristallin Solide : Les constituants élémentaires (abréviation CE) gardent une position fixe
 [PDF] cristallographie 2a mp 2016 - Unisciel
[PDF] cristallographie 2a mp 2016 - Unisciel
plan du cours de structure de la matière révision du cours de première année définition : on appelle site interstitiel ou cristallographique une cavité
 [PDF] Plan du cours Cristallographie - Chimie en PCSI
[PDF] Plan du cours Cristallographie - Chimie en PCSI
Un cristal est un arrangement triplement périodique d'atomes d'ions ou de molécules 2014 Année Internationale de la Cristallographie Premier chapitre de l'
 [PDF] Cristallographie - Physique-Chimie – BCPST
[PDF] Cristallographie - Physique-Chimie – BCPST
La cristallographie a fait beaucoup de progrès au début du 20ème siècle avec la découverte de la diffraction des rayons X par Max
 [PDF] Cours CH3 Solides cristallins - Thierry FERRARI
[PDF] Cours CH3 Solides cristallins - Thierry FERRARI
MPSI – 2018-2019 – Lycée Jeanne d'Albret D Malka CH3 – Solides cristallins Table des matières 1 Les cristaux 1 1 1 La phase solide
 [PDF] Cristallographie - cpge paradise
[PDF] Cristallographie - cpge paradise
Cristallographie »Volume de la maille V = (213)? Z (anb) Aire du poralle logrenne ? Multiplicité d'une moitk = motifs que contient cette maille :
Comment comprendre la cristallographie ?
La cristallographie est une science en grande partie expérimentale mais qui est aussi basée sur des concepts mathématiques. Elle étudie l'organisation des atomes dans la matière pour en comprendre et en utiliser les propriétés.C'est quoi la coordinence en cristallographie ?
La coordinence (ou coordinance) d'un atome central dans une molécule ou un cristal est le nombre d'atomes, molécules ou ions voisins les plus proches dans les trois directions de l'espace et reliés à cet atome central. Elle s'appelle aussi le nombre de coordination ou l'indice de coordination.C'est quoi la population d'une maille ?
? La population de la maille est le nombre d'entités (atomes, molécules ou ions) par maille, on la note en général N. ? La coordinence d'un atome est le nombre de ses plus proches voisins.- Masse volumique La masse volumique d'un solide cristallin, ? = m V , est donnée par la masse contenue dans une maille divisée par le volume d'une maille. masse volumique du fer ? (de type CFC) est de 8,21 × 103 kg/m3.

Chimie - Cristallographie PTSI
Chapitre 4
1I. Généralités sur l"état solide
Solides cristallins et solides amorphes, modèle du cristal parfaitOn appelle solide tout système qui conserve une forme propre. On distingue les solides cristallins
constitués d"une répétition quasi-parfaite de l"arrangement des atomes dans les 3 directions de
l"espace et les solides amorphes correspondant à un état liquide figé et pour lesquels l"ordre à
longue distance n"existe pas. La cristallographie est l"étude des solides cristallins ou " cristaux ».On se limite aux solides cristallins dont l"organisation sera supposé parfaitement régulière c"est à
dire sans aucun défaut : le cristal parfait (un cristal réel présente en effet de nombreux défauts).
Classification des solides cristallinsLa classification des solides cristallins repose sur la nature des liaisons qui assurent la cohésion de
l"assemblage d"atomes, de groupes d"atomes ou d"ions. On distingue alors quatre grandes familles de cristaux : - Les cristaux métalliques sont formés d"atomes métalliques et la liaison est de type métallique1. Exemples : cuivre, sodium, or etc.
- Les cristaux ioniques sont formés d"ions. À l"état solide, ces composés s"avèrent de très
mauvais conducteurs de l"électricité alors qu"ils constituent de bons conducteurs en solution.Exemples : NaCl, CsCl, Cu
2O etc.
- Les cristaux covalents où les atomes sont liés par des liaisons covalentes. Ce sont des cristaux extrêmement durs et solides. Exemples : carbone diamant, silicium, germanium etc. - Les cristaux moléculaires sont des corps simples ou composés où les molécules sont associées par des liaisons de Van der Waals. La cohésion de ce type de cristaux est faible. Exemples : gaz nobles solides, sucre, diiode, glace d"eau, cristaux organiques etc.II. Notions de base en cristallographie
Motif, réseau et noeuds Un cristal est la combinaison d"un motif et d"un réseau. Motif : c"est l"entité chimique la plus petite qui, par reproduction périodique, permet deretrouver le cristal tout entier. Un motif peut être un atome, un ensemble d"ions, une molécule. Le
motif correspond à la formule du composé.Réseau : un réseau est constitué par une infinité, triplement périodique, de points, appelés noeuds
du réseau, se déduisant les uns des autres par des translations de vecteur cwbvaut++= où cetb,a sont trois vecteurs non coplanaires et u, v, w des entiers positifs ou négatifs. Noeud : position particulière à l"intérieur du réseau où se situe un motif.1 La nature de la liaison métallique n"est pas au programme.
Chimie - Cristallographie PTSI
Chapitre 4
2 Un réseau est donc l"arrangement tridimensionnel des noeuds auxquels on associe un motif : Maille Définition Le terme générique de maille désigne tous les parallélépipèdes permettant de paver tout l"espace et de construire par translation l"ensemble des noeuds du réseau. Une maille2 est définie avec les trois
vecteurs de base cb,aet du réseau. Volume d"une maille Le volume d"une maille définie par les vecteurs cetb,a est donné par le produit mixte : ()cbaV×Ù=. Coordinence et compacité On appelle coordinence d"un atome, le nombre de plus proches voisins d"un atome considéré.On appelle
compacité d"un empilement le pourcentage de l"espace réellement occupé.Autre définition de la compacité :
maille la de volume maille la à propreen atomes lespar occupé volume=C III. Cristaux métalliques : empilements compacts de sphères identiquesLes atomes ou les ions forment de préférence des empilements à compacité élevée. On appelle
empilement compact un empilement contenant le plus de matière possible. On s"intéresse dans un2 Pour un réseau donné il peut exister plusieurs formes de mailles. Nous ne rentrerons pas dans ces distinctions et
proposeront systématiquement la maille usuelle pour chaque cristal.Motif Réseau
Cristal
Chimie - Cristallographie PTSI
Chapitre 4
3 premier temps aux cristaux métalliques dont les structures de base permettent de comprendre ensuite celles des autres cristaux (ionique et moléculaire).Un métal peut être assimilé à un réseau tridimensionnel d"ions positifs, baignant dans un gaz
d"électrons libres ou quasi-libres. On assimile en première approximation les cations métalliques à
des sphères dures. Empilement ABAB.... hexagonal compact (h.c.) Cette structure est schématisée ci-dessous :Coordinence : 12 (6 atomes tangents dans la même couche, 3 sur la couche supérieure et 3 sur la
couche inférieure).Maille : on peut considéré plusieurs mailles : un prisme droit à base hexagonale ou un primse à
base losange correspondant au tiers du précédent : Nombre d"atomes (en propre) contenus dans la maille h.c. (noté Z) : en raisonnant sur la maille de droite, on a 1 atome au centre et 8 atomes dans les sommets, chacun comptant pour un 8ème soit
28181=´+=Z.
Caractéristiques géométriques : a désignant l"arête de l"hexagone ou celle d"un losange et r le
rayon d"un atome, on a : relation entre a et r : les atomes sont tangents suivant une arête de l"hexagone : ra2=, relation entre a et c : après calculs on trouve 38=ac. Compacité de l"empilement h.c. : après calculs on trouve 74,023»p=C3, soit 74 % du volume de la maille occupé par des atomes. Masse volumique : ANVMZ VZ´=´==r
mm atomeun d© masse maille uned© volumemaille uned© masse où M est la masse molaire du corps pur cristallin considéré.3 À noter que c"est la compacité maximale pour un empilement de sphères identiques.
Chimie - Cristallographie PTSI
Chapitre 4
4 Empilement ABCABC... cubique à faces centrées (c.f.c.) Cette structure est schématisée ci-dessous :Maille : dans l"empilement cubique faces centrées les sphères se situent aux sommets d"un cube
et au centre de chaque face de ce même cube (figure de droite ci-dessus). Coordinence : 12 (idem empilement h.c.). Nombre d"atomes contenus dans la maille c.f.c. : 6 au centre de chaque face comptant pour moitié et 8 à chaque sommet comptant pour un 8ème 48
18 216=´+´=Z.
Relation entre a et r : les atomes sont tangents suivant les diagonales des faces du cube : ra42=. Compacité de l"empilement c.f.c. : idem pour l"empilement h.c. : 74,023»p=C. Empilement pseudo-compact : empilement cubique centré (c.c.) Cette structure est schématisée ci-dessous : Maille : les sphères dures d"une même couche ne sont plus tangentes mais le sont avec des sphères des couches inférieures et supérieures. Coordinence : 8 car chaque atome au centre d"une maille est tangent à 8 autres atomes. Nombre d"atomes contenus dans la maille c.c. : 1 au centre de chaque maille et 8 à chaque sommet comptant pour un 8ème 28
181=´+=Z.
Relation entre a et r : les atomes sont tangents suivant les diagonales du cube : ra43=. Compacité de l"empilement c.c. : après calculs ont rouve 74,068,083<»p=C.
Chimie - Cristallographie PTSI
Chapitre 4
5 Les sites interstitiels dans les structures cristallines.Compte tenu de la valeur de la compacité, il existe de la place dans le réseau. L"espace non-occupé
par des atomes correspond à de petites cavités appelées sites interstitiels. On se limitera ici à l"étude
des sites interstitiels de l"empilement c.f.c. à symétrie octaédrique, tétraédrique et cubique.
Définition : l"habitabilité d"un site est le rayon du plus gros atome qui puisse s"insérer dans le site
considéré sans déformer la structure. On note souvent r le rayon inséré dans le site et R le rayon des
atomes du réseau hôte. Sites à symétrie octaédrique (site O) Localisation : ils sont situés au milieu des arêtes et au centre du cube.- Nombre de sites octaédriques appartenant à la maille c.f.c. : un au centre de la maille + un au
centre de chaque arête appartenant à 4 mailles, soit 441121=´+ S.O. en propre.
Habitabilité d"un site octaédrique (site O) : les atomes du réseau hôte sont tangents le long
des diagonales des faces soit Ra42=. En notant r le rayon de l"atome qui s"insère, on trouve après calculs ()RRr414,012»-=. Sites à symétrie tétraédrique (site T) Localisation : ils sont situés au centre des 8 cubes de côté a/2 de la maille c.f.c. : - Nombre de sites tétraédriques appartenant à la maille c.f.c. : 8.Habitabilité d"un site tétraédrique (site T) : après calculs, on établitRRr225,0123»
Chimie - Cristallographie PTSI
Chapitre 4
6 Sites à symétrie cubique (site C) :Ces sites ne sont pas présents dans le cristal c.f.c., mais de géométrie suffisamment simple pour être
étudiée.
Localisation : ils sont situés au centre d"un cube de côté a : Habitabilité d"un site cubique (site C) : après calculs, on établit()RRr732,013»-=. Conditions d"insertion sans déformationIV. Cristaux ioniques
Généralités Un cristal ionique est un assemblage électriquement neutre de cations et d"anions formant undouble réseau. Chaque ion s"entoure du nombre maximal d"ions de signe opposé tels que les ions de
même signe ne soient pas en contact.Les cations (de rayon noté +r) viennent se loger dans les sites interstitiels d"un réseau d"anions
(plus gros de rayon noté -r), c"est l"entité la plus petite qui vient se placer dans les sites du réseau d"entités plus volumineuses.Pour déterminer alors quels sites (octaédrique, tétraédrique ou cubique) seront occupés de
préférence, on évalue le rapport -+rr et on le compare au rapport d"habitabilité calculéprécédemment. La petite entité occupant de préférence des cavités trop petits pour elle pour des
raisons de stabilité électrostatique, la répartition dans les sites se fait comme suit : Exemple : pour envisager une structure de type chlorure de sodium où les cations Na + occupent les sites octaédriques (O), il faut que les ions Na + s"insèrent de manière à déformer le site hôte desanions pour éviter ainsi le contact entre ions de même signe. Pour la structure NaCl on a en effet
732,0414,0££
-+rr.0,225 0,414 0,732 T,C,O C,O C Rr
0,225 0,414 0,732 T O C -+
=rr RrChimie - Cristallographie PTSI
Chapitre 4
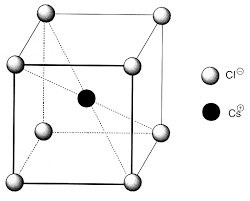
7 Structures à connaîtreCsCl NaCl (sel) ZnS (blende)
Schéma de la structure
Sites occupés par les
cations Cubique Octaédrique TétraédriqueRéseau formé par les
anions cubique simple c.f.c. c.f.c.Coordinence
anions/cations 8 6 4Relation entre +r et -r ()32arr=+-+ ()arr=+-+2 4
3arr=+
V. Cristaux covalents
Un cristal covalent est un cristal sans lequel les atomes sont unis par des liaisons covalentes. On étudie l"exemple du carbone qui existe sous plusieurs formes allotropiques parmi lesquelles le diamant et le graphite. Ces assemblages correspondent à des empilements non compacts. Carbone diamant et graphiteDiamant Graphite
Schéma de la
structureMaille du graphite
Description Structure c.f.c. d"atomes de
carbone à laquelle s"ajoute l"occupation d"un site T sur 2 pas ces mêmes atomes de carbone.Chaque C est au centre d"un
tétraèdre défini par ses 4 plus proches voisins. Empilement de plans graphitiques décalés les uns des autres et constitués par un pavage de cycles benzéniques comportant chacun 6 électrons délocalisés. À noter que les atomes de carbone sont trivalentsChimie - Cristallographie PTSI
Chapitre 4
8Nombre d"atomes par
mailles 88 18 2164=´+´+=Z Calculé sur la maille du graphite 48184142121=´++´+´+=Z
Coordinence C/C 4
Relation entre a et Cr C243ra=
Compacité 34,0163
34833=p=p´
=ar C CRemarques :
Le diamant est le composé de plus haute dureté dans l"échelle de Mohs en raison de la nature covalente des liaisons et non de sa compacité faible par rapport à celle des métaux. Le graphite met en jeu des liaisons covalentes au sein des plans et des liaisons de type van der Waals perpendiculairement aux plans moins solides que celles du diamant. Ce sont les plans graphitiques qui se " séparent » lorsqu"on écrit au crayon à mine de graphite. Le graphite n"est pas un métal mais est conducteur car il y a conduction du courantparallèlement aux plans graphitiques par les électrons délocalisés des cycles benzéniques.
VI. Cristaux moléculaires : exemple de la glaceLe motif des cristaux moléculaires est constitué par des molécules mono ou polyatomiques. Les
molécules conservent leur individualité dans le réseau cristallin. Dans le cas de la glace, il existe 12
variétés cristallines parmi lesquelles nous distinguerons la glace type diamant qui s"observe sous de
très faibles pressions et dans l"intervalle de température 148-188 K. (a = 635 pm ; OO214 3 -dadd==+ ; Z = 8)Schéma de la structure " glace diamant »
où seuls sont représentés les atomes d"oxygèneLes positions des atomes d"oxygène correspondent à celles des atomes de carbone de la structure du
diamant.La masse volumique est donnée par :
3233123
mkg.m 93410.02,610.63510.188- --=´´==rANVZM.
quotesdbs_dbs32.pdfusesText_38[PDF] les différentes formes de cybercriminalité pdf
[PDF] cycle de l'eau explication
[PDF] résumé cycle de l'eau
[PDF] les différentes étapes du cycle de l'eau
[PDF] cycle de l'eau schéma simple
[PDF] cycle de l'eau schéma ? compléter
[PDF] schéma cycle de l'eau 5ème
[PDF] cycle de l'eau cours pdf
[PDF] lalgèbre linéaire cours et exercices corrigés
[PDF] algebre generale exercices corrigés pdf
[PDF] pdf algebre premier cycle
[PDF] livre automatisme industriel pdf
[PDF] cours d'automatisme et informatique industrielle pdf
[PDF] cours de base automatisme