 Evolution spontanée dun système chimique` TP : COMPRENDRE
Evolution spontanée dun système chimique` TP : COMPRENDRE
3/ Réaliser la pile sans mettre le pont salin et relever la valeur de l'intensité du courant électrique. Appeler le professeur pour vérifier votre montage
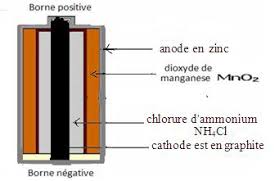 b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
l'autre demi-pile qu'on appelle aussi électrode. ○ Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de
 FICHE DE PREPARATION
FICHE DE PREPARATION
15aine de ponts salins conservés dans un becher de chlorure de puis avec seringue introduire rapidement dans le pont salin tant que la solution est tiède.
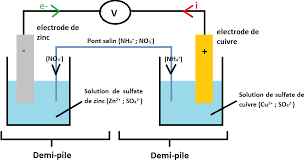 Fiche de synthèse n°4 : piles
Fiche de synthèse n°4 : piles
pont salin. Exemple : Ci-après un schéma légendé d'une pile Daniell. L'électrolyte utilisé dans le pont salin une solution de nitrate d'ammonium (NH4. + ...
 Structure et repliement des protéines - Cours 2
Structure et repliement des protéines - Cours 2
Pont salin (salt bridge ion-pairing) interaction électrostatique entre deux (ou plus) résidus chargés peut inclure des liaisons hydrogènes
 Pont salin
Pont salin
Page 1. +. - i e-. Cu(aq). 2+. SO4(aq). 2-. Zn(aq). 2+. SO4(aq). 2-. Cu(s). Zn(s). Pont salin.
 APRES EDF BDF BACTERIES DE FRANCE
APRES EDF BDF BACTERIES DE FRANCE
Des pistes futures de nouveaux paramètres : pont salin pH
 04 - Étude dune pile Ag Zn
04 - Étude dune pile Ag Zn
- dans les solutions aqueuses et dans le pont salin les porteurs de charge sont les ions : les cations se déplacent dans le sens du courant et les anions
 Piles électrochimiques
Piles électrochimiques
- Préparer un pont salin – bande de papier filtre imbibé d'une solution saline (sulfate de sodium). - Plonger les extrémités du pont salin dans les béchers et
 Electrode différentielle numérique pHD-S sc pour pH et ORP
Electrode différentielle numérique pHD-S sc pour pH et ORP
Le pont salin unique et remplaçable contient un volume considérable de solution tampon pour prolonger la durée de vie du capteur en protégeant l'électrode de
 b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de potassium (K++Cl-) qui.
 FICHE DE PREPARATION
FICHE DE PREPARATION
15aine de ponts salins conservés dans un becher de chlorure de potassium puis avec seringue introduire rapidement dans le pont salin tant que la ...
 Evolution spontanée dun système chimique` TP : COMPRENDRE
Evolution spontanée dun système chimique` TP : COMPRENDRE
Pont salin. Page 2. 2. 7/ Préciser la lame métallique qui est le siège d'une réaction de réduction. 8/ Sur le schéma ci-dessus indiquer la cathode et l'anode de
 Documents de Physique-Chimie – M. MORIN 1
Documents de Physique-Chimie – M. MORIN 1
Le pont salin sert à fermer le circuit grâce une migration d'ions qui viennent compenser les modifications de concentrations en d'ions dans les deux récipients.
 Chapitre 1
Chapitre 1
pont salin) la tension mesurée est égale à 1
 I. Principes de piles galvaniques
I. Principes de piles galvaniques
2) Les deux demi-piles sont reliées par un pont salin (ce pont est constitué du papier filtre de taille 1×8 cm mouillé avec une solution saturée de KNO3).
 T.4.1 T.P. N°1 Comment fabriquer une pile ?
T.4.1 T.P. N°1 Comment fabriquer une pile ?
Un pont salin (papier imbibé de nitrate d'ammonium). Un support en bois pour poser les béchers. III) Données : Les piles convertissent l'énergie chimique en
 lame de zinc lame dargent pont salin Ag Zn lame de zinc lame d
lame de zinc lame dargent pont salin Ag Zn lame de zinc lame d
document proposé sur le site « Sciences Physiques en BTS » : http://nicole.cortial.net lame de zinc lame d'argent pont salin.
 Piles électrochimiques
Piles électrochimiques
- Placer dans un bécher n° 2 un volume d'environ 40 mL de la solution de sulfate de cuivre et y plonger une lame de cuivre. - Préparer un pont salin – bande de
 TP N°10-PROF : LES PILES ELECTROCHIMIQUES
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
pont salin. Conclure que la pile en fonctionnement est un système hors équilibre. b) Étude du fonctionnement d'une pile en circuit ouvert.
 [PDF] c) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
[PDF] c) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de potassium (K++Cl-) qui
 [PDF] Fiche de synthèse n°4 : piles
[PDF] Fiche de synthèse n°4 : piles
Le pont salin/la membrane assure l'électroneutralité de la pile et permet de fermer le circuit électrique Dans une pile les réactifs (oxydant d'un couple et
 [PDF] tp : comprendre et modeliser le fonctionnement dune pile
[PDF] tp : comprendre et modeliser le fonctionnement dune pile
3/ Réaliser la pile sans mettre le pont salin et relever la valeur de l'intensité du courant électrique Appeler le professeur pour vérifier votre montage (
 [PDF] [PDF] Les piles - Chapitre 1
[PDF] [PDF] Les piles - Chapitre 1
Le pont salin permet de compenser les charges électriques : il y a apport d'anions vers la demi-pile dont l'électrode produit des cations (anode) et apport de
 [PDF] 10pilespdf
[PDF] 10pilespdf
La jonction entre demi-piles peut être réalisée par l'intermédiaire d'un pont salin constitué d'un tube rem- pli d'une solution gélifiée contenant des ions
 [PDF] Les piles dispositifs mettant en jeu des transformations spontanées
[PDF] Les piles dispositifs mettant en jeu des transformations spontanées
? Inversement la solution de sulfate de cuivre II s'appauvrit en ions cuivre II pour compenser ce défaut de charge positive des ions ammonium du pont salin
 Pont Salin PDF Ion Cuivre - Scribd
Pont Salin PDF Ion Cuivre - Scribd
La pile électrique chimique Il existe plusieurs types de piles électriques et la majorité d'entre elles sont des piles électriques chimiques
 [PDF] Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
[PDF] Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
Indiquer les sens de migration des ions dans le pont salin 5) Calculer à l'équilibre le potentiel de chacune des électrodes et la concentration des ions
 [PDF] cours-pc-2bac-sp-international-fr-27-1pdf - Moutamadrisma
[PDF] cours-pc-2bac-sp-international-fr-27-1pdf - Moutamadrisma
La pile Daniell est constituée de deux compartiments liés par un pont salin ? Le premier compartiment se compose d'une plaque de cuivre plongée dans une
 [PDF] I Principes de piles galvaniques
[PDF] I Principes de piles galvaniques
2) Les deux demi-piles sont reliées par un pont salin (ce pont est constitué du papier filtre de taille 1×8 cm mouillé avec une solution saturée de KNO3)
V. Électrochimie
127I. Principes de piles galvaniques
zinc métallique dans la solution qui contient des ions Zn2+ et la lame de cuivre métallique dans la solution qui contient des ions Cu2+ le symbole Zn(s) Zn2+(aq) et Cu(s)Cu2+(aq). Une lame métallique plongeant dans une solution du même ion métallique constitue une demi-pile. Si on fait relier les deux demi-piles Zn(s) Zn2+(aq) et Cu(s)Cu2+(aq)en les mettant dans deux récipients différents et en faisant circuler les électrons par un circuit extérieur, y-a-t-il des changements suivante :Activité dans la pile galvanique.
ectrons dans la pile galvanique1) Plonger la lame de cuivre métallique de taille 0,5 cm
5,0 cm dans un
bécher de 50 cm3 contenant 20 cm3de la solution de CuSO4 à 1 mol/dm3, écrire ensuite Cu(s)Cu2+(aq) sur le bécher et plonger la lame de zinc métallique de taille 0,5 cm5,0 cm dans un bécher de 50 cm3 contenant 20 cm3 de la
solution de ZnSO4 à 1 mol/dm3 Zn(s) Zn2+(aq) sur le bécher.2) Les deux demi-piles sont reliées par un pont salin (ce pont est constitué du
papier filtre de taille 18 cm mouillé avec une solution saturée de KNO3).Chaque
extrémité du pont salin est plongée dans chacun des deux béchers.V. Électrochimie
1283) Relier la lame de cuivre et la lame
la différence de potentiel.4) Échanger les bornes des électrodes, observer
différence de potentiel.5) Relier maintenant électriquement les électrodes à une petite lampe
électrique
6) Refaire les mêmes expériences comme les étapes 1 4 mais en utilisant
les couples des deux demi-piles ci-dessous et changer le pont salin pour chaque expérience.Cu(s)Cu2+(aq)et Mg(s)Mg2+(aq)
Zn(s) Zn2+(aq)et Mg(s)Mg2+(aq)
Cu(s)Cu2+(aq) et Fe(s)Fe2+(aq)
Zn(s) Zn2+(aq)et Fe(s)Fe2+(aq)
Fe(s)Fe2+(aq)et Mg(s)Mg2+(aq)
-piles sont reliées par un pont salin, qui3. Le pont salin
s solutions de chaque demi-pile. Les deux électrodes des piles sont reliées à un se déplace de même sens que les électrons. Quand les deux demi-piles sont reliées par un fil électrique permettant aux ions de se déplacer, et un autre fil pour les déplacements des ions positifs et négatifs, on obtient une pile galvanique. Le métal immergé dans la solution de chaque demi-pile constitue une électrode. demi-pilesZn(s) Zn2+(aq) et Cu(s)Cu2+(aq) avec un circuit complet. Le pont salin sépare les deux solutions et les électrodes sont reliées par un fil conducteur sur lequel est disposé un ampèremètre. zinc. Le courant électrique ne se déplaçant que du pôle positif vers du pôle négatif, o de cuivre constitue le pôle positif de la pile et Les électrons circulent dans le sens inverse du courant électrique, donc de la lame de zinc vers la lame de cuivre.V. Électrochimie
129anode ions Zn2+ en solution : Zn(s) o
Zn2+(aq) + 2 e
e. cathode provenant du circuit extérieur et se transforme :Cu2+ (aq) + 2 e
oCu (s)
La solution perd alors sa couleur bleue caractéristique des ions Cu2+ et unZn(s) +Cu2+(aq)
oZn2+(aq) + Cu(s)
Figure 21.2 Représentation des réactions de la pile galvaniqueV. Électrochimie
130II. Représentation schématique galvanique
Pour décrire les piles galvaniques, on utilise la représentation schématique, -piles Zn(s) Zn2+(aq) et Cu(s)Cu2+(aq), le changement :Zn(s) +Cu2+(aq)
oZn2+(aq) + Cu(s)
La repré
Zn(s)Zn2+(aq, 1 mol/dm3)quotesdbs_dbs35.pdfusesText_40[PDF] electrode 1ere espece
[PDF] électrode au chlorure d'argent
[PDF] electrode de platine
[PDF] électrode d'argent
[PDF] électrode de référence au chlorure d'argent
[PDF] montage électrochimique 3 électrodes
[PDF] comment tracer une courbe courant potentiel
[PDF] montage ? trois électrodes
[PDF] comment tracer courbe intensité potentiel
[PDF] exercice courbe intensité-potentiel
[PDF] tracé des courbes ie de fe2+/fe3+
[PDF] courbe intensité potentiel exercices corrigés
[PDF] eeg interpretation
[PDF] eeg interpretation pdf
