 Evolution spontanée dun système chimique` TP : COMPRENDRE
Evolution spontanée dun système chimique` TP : COMPRENDRE
3/ Réaliser la pile sans mettre le pont salin et relever la valeur de l'intensité du courant électrique. Appeler le professeur pour vérifier votre montage
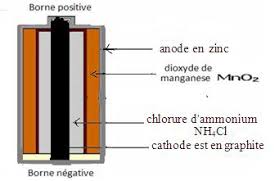 b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
l'autre demi-pile qu'on appelle aussi électrode. ○ Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de
 FICHE DE PREPARATION
FICHE DE PREPARATION
15aine de ponts salins conservés dans un becher de chlorure de puis avec seringue introduire rapidement dans le pont salin tant que la solution est tiède.
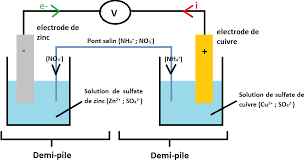 Fiche de synthèse n°4 : piles
Fiche de synthèse n°4 : piles
pont salin. Exemple : Ci-après un schéma légendé d'une pile Daniell. L'électrolyte utilisé dans le pont salin une solution de nitrate d'ammonium (NH4. + ...
 Structure et repliement des protéines - Cours 2
Structure et repliement des protéines - Cours 2
Pont salin (salt bridge ion-pairing) interaction électrostatique entre deux (ou plus) résidus chargés peut inclure des liaisons hydrogènes
 Pont salin
Pont salin
Page 1. +. - i e-. Cu(aq). 2+. SO4(aq). 2-. Zn(aq). 2+. SO4(aq). 2-. Cu(s). Zn(s). Pont salin.
 APRES EDF BDF BACTERIES DE FRANCE
APRES EDF BDF BACTERIES DE FRANCE
Des pistes futures de nouveaux paramètres : pont salin pH
 04 - Étude dune pile Ag Zn
04 - Étude dune pile Ag Zn
- dans les solutions aqueuses et dans le pont salin les porteurs de charge sont les ions : les cations se déplacent dans le sens du courant et les anions
 Piles électrochimiques
Piles électrochimiques
- Préparer un pont salin – bande de papier filtre imbibé d'une solution saline (sulfate de sodium). - Plonger les extrémités du pont salin dans les béchers et
 Electrode différentielle numérique pHD-S sc pour pH et ORP
Electrode différentielle numérique pHD-S sc pour pH et ORP
Le pont salin unique et remplaçable contient un volume considérable de solution tampon pour prolonger la durée de vie du capteur en protégeant l'électrode de
 b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
b) Fonctionnement de la pile Daniell : c) Réaction aux électrodes: d
Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de potassium (K++Cl-) qui.
 FICHE DE PREPARATION
FICHE DE PREPARATION
15aine de ponts salins conservés dans un becher de chlorure de potassium puis avec seringue introduire rapidement dans le pont salin tant que la ...
 Evolution spontanée dun système chimique` TP : COMPRENDRE
Evolution spontanée dun système chimique` TP : COMPRENDRE
Pont salin. Page 2. 2. 7/ Préciser la lame métallique qui est le siège d'une réaction de réduction. 8/ Sur le schéma ci-dessus indiquer la cathode et l'anode de
 Documents de Physique-Chimie – M. MORIN 1
Documents de Physique-Chimie – M. MORIN 1
Le pont salin sert à fermer le circuit grâce une migration d'ions qui viennent compenser les modifications de concentrations en d'ions dans les deux récipients.
 Chapitre 1
Chapitre 1
pont salin) la tension mesurée est égale à 1
 I. Principes de piles galvaniques
I. Principes de piles galvaniques
2) Les deux demi-piles sont reliées par un pont salin (ce pont est constitué du papier filtre de taille 1×8 cm mouillé avec une solution saturée de KNO3).
 T.4.1 T.P. N°1 Comment fabriquer une pile ?
T.4.1 T.P. N°1 Comment fabriquer une pile ?
Un pont salin (papier imbibé de nitrate d'ammonium). Un support en bois pour poser les béchers. III) Données : Les piles convertissent l'énergie chimique en
 lame de zinc lame dargent pont salin Ag Zn lame de zinc lame d
lame de zinc lame dargent pont salin Ag Zn lame de zinc lame d
document proposé sur le site « Sciences Physiques en BTS » : http://nicole.cortial.net lame de zinc lame d'argent pont salin.
 Piles électrochimiques
Piles électrochimiques
- Placer dans un bécher n° 2 un volume d'environ 40 mL de la solution de sulfate de cuivre et y plonger une lame de cuivre. - Préparer un pont salin – bande de
 TP N°10-PROF : LES PILES ELECTROCHIMIQUES
TP N°10-PROF : LES PILES ELECTROCHIMIQUES
pont salin. Conclure que la pile en fonctionnement est un système hors équilibre. b) Étude du fonctionnement d'une pile en circuit ouvert.
 [PDF] c) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
[PDF] c) Réaction aux électrodes: d) Rôle du pont salin - AlloSchool
Le pont salin (ou ionique) qui relie les deux solutions il est constitué d'une solution de chlorure de potassium (K++Cl-) qui
 [PDF] Fiche de synthèse n°4 : piles
[PDF] Fiche de synthèse n°4 : piles
Le pont salin/la membrane assure l'électroneutralité de la pile et permet de fermer le circuit électrique Dans une pile les réactifs (oxydant d'un couple et
 [PDF] tp : comprendre et modeliser le fonctionnement dune pile
[PDF] tp : comprendre et modeliser le fonctionnement dune pile
3/ Réaliser la pile sans mettre le pont salin et relever la valeur de l'intensité du courant électrique Appeler le professeur pour vérifier votre montage (
 [PDF] [PDF] Les piles - Chapitre 1
[PDF] [PDF] Les piles - Chapitre 1
Le pont salin permet de compenser les charges électriques : il y a apport d'anions vers la demi-pile dont l'électrode produit des cations (anode) et apport de
 [PDF] 10pilespdf
[PDF] 10pilespdf
La jonction entre demi-piles peut être réalisée par l'intermédiaire d'un pont salin constitué d'un tube rem- pli d'une solution gélifiée contenant des ions
 [PDF] Les piles dispositifs mettant en jeu des transformations spontanées
[PDF] Les piles dispositifs mettant en jeu des transformations spontanées
? Inversement la solution de sulfate de cuivre II s'appauvrit en ions cuivre II pour compenser ce défaut de charge positive des ions ammonium du pont salin
 Pont Salin PDF Ion Cuivre - Scribd
Pont Salin PDF Ion Cuivre - Scribd
La pile électrique chimique Il existe plusieurs types de piles électriques et la majorité d'entre elles sont des piles électriques chimiques
 [PDF] Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
[PDF] Oxydo-réduction et Piles électrochimiques SMPC2 fsr 2015
Indiquer les sens de migration des ions dans le pont salin 5) Calculer à l'équilibre le potentiel de chacune des électrodes et la concentration des ions
 [PDF] cours-pc-2bac-sp-international-fr-27-1pdf - Moutamadrisma
[PDF] cours-pc-2bac-sp-international-fr-27-1pdf - Moutamadrisma
La pile Daniell est constituée de deux compartiments liés par un pont salin ? Le premier compartiment se compose d'une plaque de cuivre plongée dans une
 [PDF] I Principes de piles galvaniques
[PDF] I Principes de piles galvaniques
2) Les deux demi-piles sont reliées par un pont salin (ce pont est constitué du papier filtre de taille 1×8 cm mouillé avec une solution saturée de KNO3)
T.4.1 T.P. N°1 Comment fabriquer une pile ?
I) Objectif :
L'objectif de ce T.P. est de mettre en évidence les constituants d'une pile.II) Matériel :
Deux béchers étiquetés " Cu »
Un bécher étiqueté " Zn »
Une lame de zinc, deux lames de cuivre
Une solution de sulfate de zinc (1 mol/L)
Une solution de sulfate de cuivre (1 mol/L)
Un voltmètre (multimètre)
Deux fils de connexion (un rouge, un noir)
Deux pinces crocodiles
Un pont salin (papier imbibé de nitrate d'ammonium)Un support en bois pour poser les béchers
III) Données :
Les piles convertissent l'énergie chimique en énergie électrique grâce à un transfert spontané d'électrons qui se produit entre deux couples oxydant-réducteur. Les deux couples oxydant-réducteur n'étant pas en contact direct, le transfert d'électrons s'effectue par l'intermédiaire du circuit électrique extérieur.IV) Protocole expérimental :
Remplir le bécher " Zn » aux deux tiers avec la solution de sulfate de zinc 1 mol/L. Remplir l'un des béchers " Cu » aux deux tiers avec la solution de sulfate de cuivre1 mol/L.
Réaliser le montage 1, le voltmètre étant réglé sur " 20 V » en courant continu.Montage 1
Sulfate de
zincSulfate de
cuivreLame de
zincLame de
cuivreVoltmètre
T41 TP N°1 Comment fabriquer une pile Page 2 / 3 Noter la valeur lue sur le voltmètre : U = V. Mettre en place le pont salin (papier imbibé de nitrate d'ammonium) comme le montre le montage 2.Montage 2
Sulfate de
zincSulfate de
cuivreLame de
zincLame de
cuivreVoltmètre
Pont salin
Noter la valeur lue sur le voltmètre : U = V. Remplir l'autre béchers " Cu » aux deux tiers avec la solution de sulfate de cuivre1 mol/L.
Réaliser le montage 3 avec le pont salin (on remplace le bécher contenant le sulfate de zinc par le bécher contenant du sulfate de cuivre dans lequel on insère l'autre lame de cuivre)Montage 3
Sulfate de
cuivreSulfate de
cuivreLame de
cuivreLame de
cuivreVoltmètre
Pont salin
Noter la valeur lue sur le voltmètre : U = V.V) Observation :
T41 TP N°1 Comment fabriquer une pile Page 3 / 3Lors du montage 1, le voltmètre indique V. Vous réalisé une pile. En
ajoutant le pont salin, le voltmètre indique V (montage 2). Vous réalisé
une pile. Cette tension correspond à la force électromotrice (f.e.m.) de la pile, c'est la tension mesurée aux bornes d'une pile qui ne débite pas de courant.Pour le montage 3, le voltmètre indique V. Vous réalisé une pile. En
effet les lames que l'on appelle dans ce cas doivent être de nature
Le voltmètre mesure une tension positive, cela permet de définir lesdes bornes. L'électrode de correspond à la borne + et l'électrode de
à la borne -.
VI) Explication :
Le voltmètre du montage 2 permet d'affirmer que les électrons circulent de la lame de zinc à la lame de cuivre. (On rappelle que le sens conventionnel du courant électrique est du + vers le - à l'extérieur de la pile). À l'anode, c'est-à-dire au pôle négatif de la pile, les atomes de zinc sont oxydés:Zn à Zn2+ + 2e- .
Les électrons libérés par les atomes de zinc parcourent le circuit, puis réagissent avec les ions cuivre II :Cu2+ + 2e- à Cu.
À la cathode, les ions Cu2+ sont réduits.
Le bilan global s'écrit :
Zn + Cu2+ à Zn2+ + Cu.
C'est une réaction d'oxydoréduction spontanée. Le montage 3 n'est pas une pile. Pour fabriquer une pile, il est nécessaire que les deuxélectrodes soient de nature différente.
La pile fabriquée ici se nomme pile Daniell.
quotesdbs_dbs35.pdfusesText_40[PDF] electrode 1ere espece
[PDF] électrode au chlorure d'argent
[PDF] electrode de platine
[PDF] électrode d'argent
[PDF] électrode de référence au chlorure d'argent
[PDF] montage électrochimique 3 électrodes
[PDF] comment tracer une courbe courant potentiel
[PDF] montage ? trois électrodes
[PDF] comment tracer courbe intensité potentiel
[PDF] exercice courbe intensité-potentiel
[PDF] tracé des courbes ie de fe2+/fe3+
[PDF] courbe intensité potentiel exercices corrigés
[PDF] eeg interpretation
[PDF] eeg interpretation pdf
