 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Liqueur de Fehling. Solution 1. CuSO4 5H2O. 40 g. Eau. 300 mL. (prévoir un excès de 5-10% de CuSO4). Solution 2. NaOH. 130 g. Tartrate de K et Na. 160 g. Eau.
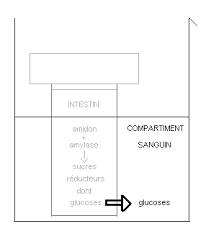 Kit dialyse
Kit dialyse
sucres réducteurs à l'aide de réactions au lugol et à la liqueur de Fehling A + B. L'autre groupe réalise la digestion In Vitro en mettant de l'amidon en ...
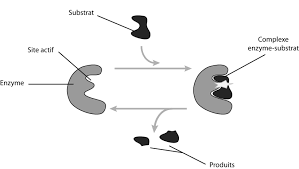 Sans titre
Sans titre
Ces oses se comportent comme des réducteurs : ils réduisent la liqueur de Fehling à C'est un sucre réducteur. ◗. Le lactose formé d'une molécule de glucose ...
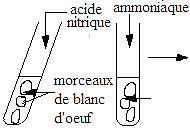 CODE: SVT DURÉE : 6H
CODE: SVT DURÉE : 6H
Le sucre réducteur du pain est le glucose et le sucre réducteur du lait est le lactose. La liqueur de Fehling qui permet de caractériser les sucres réducteurs
 Fiche technique dutilisation de réactifs spécifiques de différents
Fiche technique dutilisation de réactifs spécifiques de différents
- Verser ........ mL de la solution dans un tube à essais
 TP 2 : De lamidon au maltose une simplification moléculaire Mise
TP 2 : De lamidon au maltose une simplification moléculaire Mise
- liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL) à température ambiante. - solution d
 Observations sur la méthode de Gabriel Bertrand pour le dosage
Observations sur la méthode de Gabriel Bertrand pour le dosage
8 oct. 2019 comme officielle qui consiste à oxyder le sucre réducteur au moyen d'une liqueur du type Barreswill-Fehling
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
déduire la quantité d'oses réducteurs totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Test à la liqueur de Fehling : mise en évidence des sucres réducteurs. La liqueur de Fehling est une solution renfermant des ions Cu2+ de couleur bleue en
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling. Le document 1 nous rappelle que la présence de sucres réducteurs (glucose et maltose) traduit l'hydrolyse des polysaccharides. On en ...
 dosage des sucres réducteurs: méthode de Fehling
dosage des sucres réducteurs: méthode de Fehling
Pour une même quantité de solution de liqueur de Fehling utilisée soit 5 mL
 Sans titre
Sans titre
C'est le sucre de table ou sucre blanc. Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling.
 Dosage des glucides présents dans un jus de fruit
Dosage des glucides présents dans un jus de fruit
totalité une prise d'essai équivalente de liqueur de Fehling. Par comparaison on en déduit la teneur en sucre réducteur de la solution à.
 Kit dialyse
Kit dialyse
Réactif. Couleur. LUGOL. LIQUEUR DE FEHLING A + B. Chauffée au bain-marie. Du réactif. Avec ajout de sucres réducteurs. Avec ajout d'amidon
 TP 2 : De lamidon au maltose une simplification moléculaire Mise
TP 2 : De lamidon au maltose une simplification moléculaire Mise
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL) à température ambiante.
 1 L A 04 Les glucides B version prof
1 L A 04 Les glucides B version prof
Dans un tube à essai contenant de la liqueur de Fehling de couleur bleue L'acide chlorhydrique transforme le saccharose en sucres réducteurs : glucose ...
 Expérience de biochimie : Analyser des aliments Biologie
Expérience de biochimie : Analyser des aliments Biologie
Biochimie : liqueur de Fehling lugol
 Atelier de biologie mise en évidence de glucides
Atelier de biologie mise en évidence de glucides
présence de différents sucres dans les aliments. Durée de l'activité. 1 séance indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling.
 TP 2 : La spécificité des enzymes digestives. Mise en situation et
TP 2 : La spécificité des enzymes digestives. Mise en situation et
liqueur de Fehling (réactif spécifique des sucres réducteurs comme le maltose). - solution d'amylase (+ pipette 5 mL). - eau distillée.
 MÉMOIRE DE MASTER
MÉMOIRE DE MASTER
Dosage des sucres réducteurs. A) Principe. Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs.
 [PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
[PDF] dosage des sucres réducteurs: méthode de Fehling - Sites ENSFEA
Liqueur de Fehling Solution 1 CuSO4 5H2O 40 g Eau 300 mL (prévoir un excès de 5-10 de CuSO4) Solution 2 NaOH 130 g Tartrate de K et Na 160 g Eau
 Dosage des sucres réducteurs par la méthode de Fehling
Dosage des sucres réducteurs par la méthode de Fehling
Cette méthode de dosage repose sur la réduction de la liqueur de Fehling mélange d'une solution de sulfate de cuivre et de sel de Seignette en présence de
 Des sucres réducteurs - Mettre en évidence - Académie de Versailles
Des sucres réducteurs - Mettre en évidence - Académie de Versailles
La liqueur de Fehling renferme des ions cuivre II de couleur bleue A chaud en présence d'un réducteur se forme un précipité rouge brique d'oxyde de cuivre
 [PDF] Fiche technique dutilisation de réactifs spécifiques de différents
[PDF] Fiche technique dutilisation de réactifs spécifiques de différents
A chaud et en présence de glucides réducteurs la liqueur de Fehling donne un précipité rouge brique d'oxyde de cuivre Cu2O A : Couleur initial du réactif ;
 [PDF] MÉMOIRE DE MASTER - University of Biskra Repository
[PDF] MÉMOIRE DE MASTER - University of Biskra Repository
Cette méthode basée sur la réduction de le liqueur de Fehling par les sucres réducteurs contenus dans l'échantillon (Audigier et al 1984) 3 3 1 10
 [PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
[PDF] Atelier de biologie mise en évidence de glucides - Franciaoktataseu
Elle permet aussi de présenter aux jeunes deux indicateurs colorés le lugol (l'eau iodée) et la liqueur de Fehling Remarque : Cette expérience est très prisée
 [PDF] Les molécules organiques
[PDF] Les molécules organiques
C'est le sucre de table ou sucre blanc Il n'est pas réducteur et ne peut donc pas être mis en évidence par la réaction à la liqueur de Fehling
 [PDF] Chimie des sucrespdf - ORBi
[PDF] Chimie des sucrespdf - ORBi
Les OSES encore appelés monosaccharides ou sucres simples sont les plus simples des glucides Ils sont REDUCTEURS Les sures simples sont des chaînes carbonées
 [PDF] 1 L A 04 Les glucides B version prof
[PDF] 1 L A 04 Les glucides B version prof
Interprétation : certains sucres comme le glucose réagissent avec la liqueur de Fehling ; ils sont appelés "sucres réducteurs"
 [PDF] TP 21 : Dosage du glucose
[PDF] TP 21 : Dosage du glucose
Le glucose réagit à chaud avec la liqueur de Fehling La transformation est visualisée par un changement de couleur : la teinte du mélange vire du bleu au
Pourquoi le glucose réagit avec la liqueur de Fehling ?
La raison est que le saccharose s'hydrolyse en fructose et en glucose, et que ce dernier réagit avec les ions cuivre(II) de la liqueur.Pourquoi le sucre est réducteur ?
Les sucres réducteurs sont des sucres simples donneurs d'électrons dans une réaction d'oxydo-réduction. Par exemple le glucose, le fructose et le maltose. Ils poss?nt une fonction aldéhyde. Les sucres non réducteurs ne poss?nt pas cette fonction aldéhyde.Comment mettre en évidence le sucre réducteur ?
Mettre la substance à tester en solution dans un tube à essai avec de l'eau distillée. Faire chauffer au bec bunsen ou mieux mettre au bain-marie à 100°C quelques minutes. La formation d'un précipité rouge brique indique la présence de sucres réducteurs.- On utilise la liqueur de Fehling pour caractériser les aldéhydes aliphatiques (la réaction est moins nette pour les aldéhydes aromatiques), tel le glucose. La réaction provoque la formation d'un précipité d'oxyde cuivreux rouge-brun. On l'utilise aussi pour déterminer la proportion de sucres réducteurs.